
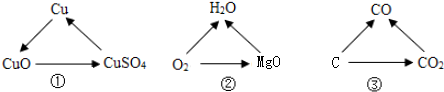
| A. | ①②③ | B. | ①② | C. | ①③ | D. | ②③ |
分析 一步反应实现即原物质只发生一个反应即可转化为目标物质,根据所涉及物质的性质,分析能否只通过一个反应而实现即可.
解答 解:①铜与氧气在加热条件下生成氧化铜,氧化铜与稀硫酸反应生成硫酸铜和水,铁与硫酸铜溶液反应生成硫酸亚铁溶液和铜,一定条件下均能一步实现.
②氢气在氧气中燃烧生成水,镁在氧气中燃烧生成氧化镁,氢气与氧化镁反应生成镁和水,一定条件下均能一步实现.
③碳不充分燃烧生成一氧化碳,碳充分燃烧生成二氧化碳,二氧化碳与碳在高温下反应生成一氧化碳,一定条件下均能一步实现.
故①②③一定条件下均能一步实现.
故选:A.
点评 本题有一定难度,熟练掌握所涉及物质的性质、抓住关键词“能否一步实现”是解决此类问题的关键.


 发散思维新课堂系列答案
发散思维新课堂系列答案科目:初中化学 来源: 题型:解答题
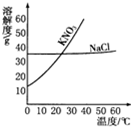 根据如图中KNO3和NaCl的溶解度曲线,回答下列问题.
根据如图中KNO3和NaCl的溶解度曲线,回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| 取一定量纯碱样品配成溶液后,滴加过量的CaCl2溶液. | 产生白色沉淀 | 反应的化学方程式: Na2CO3+CaCl2=CaCO3+2NaCl |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 归类 | 物质或微粒 |
| A | 三大合成材料 | 塑料、合成橡胶、合成纤维 |
| B | 三大化石燃料 | 煤、石油、天然气 |
| C | 构成物质的三大微粒 | 分子、原子、离子 |
| D | 同一物质的三个俗名 | 火碱、烧碱、纯碱 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 谷氨酸钠相对分子质量为169 | |
| B. | 谷氨酸钠是由5个碳原子、8个氢原子、4个氧原子、1个氮原子和1个钠原子构成 | |
| C. | 20℃时,100g水最多可配制成171.7g谷氨酸钠的饱和溶液 | |
| D. | 谷氨酸钠中钠元素的质量分数约为13.6% |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
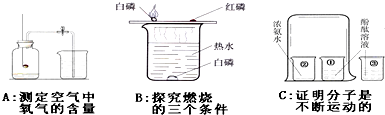
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com