
分析 (1)根据实验室制取氧气的反应有过氧化氢在二氧化锰的催化作用下生成水和氧气,氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气进行分析;
(2)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析;
(3)根据锌和盐酸反应生成硫酸锌和氢气进行分析;
(4)根据木炭和氧化铜在高温的条件下反应生成铜和二氧化碳进行分析;
(5)根据二氧化碳和木炭在高温的条件下反应生成一氧化碳进行分析;
(6)根据一氧化碳和氧化铁在高温的条件下反应生成铁和二氧化碳进行分析;
(7)根据盐酸和氧化铁反应生成氯化铁和水进行分析;
(8)根据氢氧化钠和二氧化碳反应生成碳酸钠和水进行分析;
(9)根据氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水进行分析;
(10)根据氢氧化钠和硫酸反应生成硫酸钠和水进行分析;
(11)根据氧化钙和水反应生成氢氧化钙进行分析;
(12)根据二氧化碳和水反应生成碳酸进行分析;
(13)根据铁和硫酸铜反应生成硫酸亚铁和铜进行分析;
(14)根据盐酸和碳酸钠反应生成氯化钠、水和二氧化碳进行分析.
解答 解:(1)实验室制取氧气的反应有过氧化氢在二氧化锰的催化作用下生成水和氧气,氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,三个反应满足分解反应一变多的条件,属于分解反应,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,属于复分解反应,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)锌和盐酸反应生成硫酸锌和氢气,属于置换反应,化学方程式为:Zn+H2SO4=ZnSO4+H2↑;
(4)木炭和氧化铜在高温的条件下反应生成铜和二氧化碳,化学方程式为:C+2CuO$\frac{\underline{\;高温\;}}{\;}$CO2↑+2Cu;
(5)二氧化碳和木炭在高温的条件下反应生成一氧化碳,化学方程式为:CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;
(6)一氧化碳和氧化铁在高温的条件下反应生成铁和二氧化碳,化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(7)盐酸和氧化铁反应生成氯化铁和水,化学方程式为:6HCl+Fe2O3=2FeCl3+3H2O;
(8)氢氧化钠和二氧化碳反应生成碳酸钠和水,化学方程式为:2NaOH+CO2=Na2CO3+H2O;
(9)氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
(10)氢氧化钠和硫酸反应生成硫酸钠和水,化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
(11)氧化钙和水反应生成氢氧化钙,化学方程式为:CaO+H2O=Ca(OH)2;
(12)二氧化碳和水反应生成碳酸,化学方程式为:CO2+H2O=H2CO3;
(13)铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4=FeSO4+Cu;
(14)盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,化学方程式为:2HCl+Na2CO3=2NaCl+H2O+CO2↑.
故答案为:(1)分解反应,2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)复分解,CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)置换,Zn+H2SO4=ZnSO4+H2↑;
(4)C+2CuO$\frac{\underline{\;高温\;}}{\;}$CO2↑+2Cu;
(5)CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;
(6)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(7)6HCl+Fe2O3=2FeCl3+3H2O;
(8)2NaOH+CO2=Na2CO3+H2O;
(9)Ca(OH)2+CO2=CaCO3↓+H2O;
(10)Ca(OH)2+CO2=CaCO3↓+H2O;
(11)CaO+H2O=Ca(OH)2;
(12)CO2+H2O=H2CO3;
(13)Fe+CuSO4=FeSO4+Cu;
(14)2HCl+Na2CO3=2NaCl+H2O+CO2↑.
点评 在解此类题时,首先分析应用的原理,然后找出反应物、生成物,最后结合方程式的书写规则书写方程式.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | 相同温度下,甲的溶解度比乙的大,则甲溶液的溶质的质量分数比乙溶液的大 | |
| B. | KNO3溶于水时溶液温度无明显变化,则NH4NO3溶于水时溶液温度也无明显变化 | |
| C. | 点燃H2与O2混合气体可能爆炸,则点燃CH4与O2的混合气体也可能爆炸 | |
| D. | CaO能与水反应,则CuO也能与水反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 实验装置 | 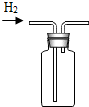 | 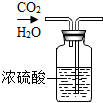 | 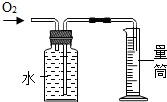 | 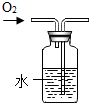 |
| 解释 | 用于排空气法收集氢气的装置 | 用于干燥二氧化碳的装置 | 用于测量氧气体积的装置 | 用于医院给病人供氧气的装置 |
| 选项 | A | B | C | D |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
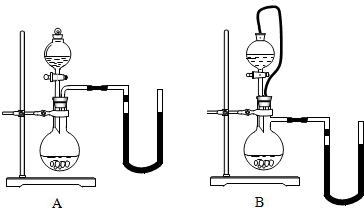
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
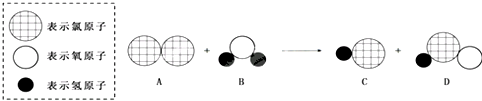
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
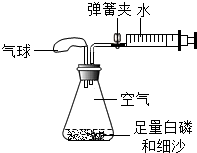 课外活动小组的同学们利用锥形瓶、注射器、白磷等仪器和药品,对“测定空气里氧气含量”进行了创新实验探究.
课外活动小组的同学们利用锥形瓶、注射器、白磷等仪器和药品,对“测定空气里氧气含量”进行了创新实验探究.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com