
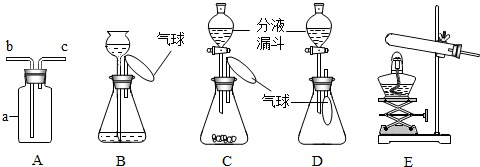
分析 (1)根据仪器装置图和检查装置气密性的方法解答;
(2)根据实验室制氧气的原理进行分析解答;
(3)根据二氧化碳的化学性质分析解答.
解答 解:(1)根据仪器装置图可知a仪器是集气瓶,向B中加水会看到气球胀大,说明该装置气密性良好;
(2)C、E均属于固液常温型制气装置,制取氧气时用过氧化氢分解制氧气可用此类装置,过氧化氢在二氧化锰做催化剂的条件下分解生成水和氧气;氧气的密度比空气大收集时要从用向上排空气法,故氧气从b导入;
(3)二氧化碳能被碱溶液吸收使装置内气体压强变小,在外界大气压的作用下,小气球会鼓起来.
故答案为:(1)集气瓶;良好;(2)H2O2;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;b;(3)②.
点评 此题的难度不大,掌握实验室制取氧气的原理以及二氧化碳的性质等即可顺利解答此题.


科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 如图是A、B、C三种物质的溶解度曲线,其中正确的是( )
如图是A、B、C三种物质的溶解度曲线,其中正确的是( )| A. | t1℃时,等质量的A、B、C三种物质的溶液中溶质质量分数关系为C>A=B | |
| B. | 在t2℃时,A、C两种物质的饱和溶液中,所含溶质质量相等 | |
| C. | 若t1℃时,A物质的溶解度为25g,则在此温度下,该物质的溶液中溶质质量分数最大不会超过20% | |
| D. | t1℃时,将A、B、C三种物质的饱和溶液升温到t3℃,所得溶液中溶质的质量分数由大到小的顺序为A>B=C |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 某校化学小组在利用盐酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象如图所示.下列说法正确的是( )
某校化学小组在利用盐酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象如图所示.下列说法正确的是( )| A. | 图中c点所示的溶液呈碱性 | |
| B. | 图中a点所示溶液中,含有的溶质是NaCl和HCl | |
| C. | 由b点到c点,溶液的酸性减弱 | |
| D. | b点所示酸和碱恰好完全反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 3个水分子:3H2O | B. | 镁离子Mg+2 | C. | 2个氢分子:2H | D. | 2个氧原子:O2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 钛酸亚铁(FeTiO3)中钛元素为+3价 | |
| B. | ①中反应为:2FeTiO3+6C+7Cl2$\frac{\underline{\;一定条件\;}}{\;}$2X+2TiCl4+6CO,则X为FeCl2 | |
| C. | ②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为1:2 | |
| D. | ③中氩气(Ar)作保护气,反应类型为置换反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
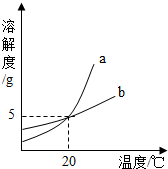 如图是a、b两种固体物质的溶解度曲线,下列说法中正确的是( )
如图是a、b两种固体物质的溶解度曲线,下列说法中正确的是( )| A. | 20oC时,将100g a的饱和溶液蒸干可以得到5g a物质 | |
| B. | 在20℃时,a、b溶液中溶质的质量分数相同 | |
| C. | Ca(OH)2的溶解度曲线与b相似 | |
| D. | 从a的饱和溶液得到a物质的大量固体可以用冷却的方法 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com