
| A. | ②⑤ | B. | ②③ | C. | ③⑥ | D. | ②④ |
分析 根据实验操作方法、物质的性质以及实验的注意事项进行分析解答即可.
解答 解:①可燃气不纯时点燃或加热可能产生爆炸,故在点燃H2、CO、CH4等易燃气体前,必须检验气体的纯度,正确;
②在稀释浓硫酸时将浓硫酸沿器壁慢慢注入水中,并用玻璃棒搅拌,错误;
③用玻璃棒蘸取待测液滴在pH试纸上,变色后与标准比色卡对比读数,正确;
④给试管中液体加热,液体一般不超过试管容积的$\frac{1}{3}$,正确;
⑤称量氢氧化钠固体药品时,要将氢氧化钠固体放在烧杯中,不能放在纸上,错误;
⑥检查气密性时应先将导管放入水中再手握试管,正确;
故选:A.
点评 本题考查的是实验操作中的注意事项,完成此题,可以依据已有的实验操作进行.


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:初中化学 来源: 题型:推断题
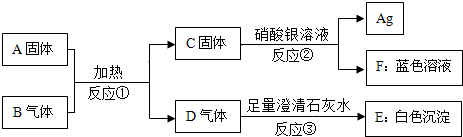
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 蜘蛛吐丝 | B. | 蚂蚁觅食 | C. | 黄莺啼唱 | D. | 蜜蜂传粉 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
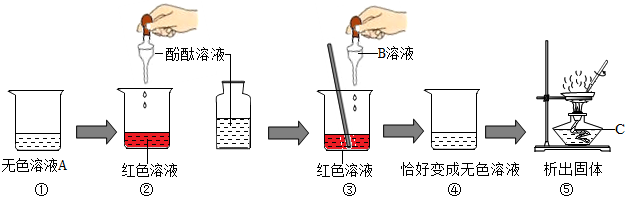
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 二氧化碳和水 | B. | 盐酸和硝酸银溶液 | ||
| C. | 铝和稀硫酸 | D. | 氢氧化钾溶液和稀硫酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
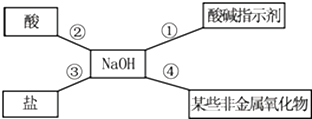
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验方案 | 实验操作 | 实验现象 | 实验结论 |
| 方案一 | 取甲组反应后溶液,滴加过量碳酸钠溶液 | 有气泡产生 | 反应后硫酸溶液过量 |
| 方案二 | 取少量甲组反应后溶液,滴在pH试纸上, | 试纸变色,对比比色卡,pH<7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com