
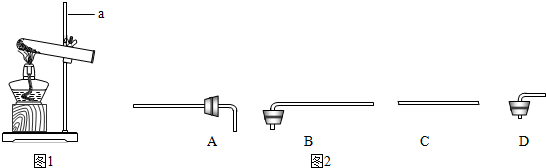
分析 ①根据实验室常见仪器的名称填空;
②本反应是蓝色胆矾加热分解为白色的硫酸铜粉末;
③为了能把试管中的空气排净,避免发生爆炸,应该选择不带橡皮塞的导管;
④根据氢气还原氧化铜的实验步骤以及注意事项进行解答;
⑤从氢气和一氧化碳两者是否有毒性分析判断;
⑥根据实验室制取氧气的反应物、生成物以及反应条件书写化学方程式;由氧气的助燃性选择验满的方法.
解答 解:①仪器a的名称是铁架台;故填:铁架台;
②蓝色的胆矾(CuSO4•5H2O失水后变为白色粉末硫酸铜(CuSO4);故填:由蓝色变成白色;
③用氢气还原氧化铜的实验中,导管上的橡皮塞要除去,导管还要伸到试管底部药品上方;氢气还原氧化铜时,氢气+氧化铜→铜+水;
故填:C;底;H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$H2O+Cu;
④反应结束后必须先熄灭酒精灯,后停止通氢气,否则生成的红色固体铜又会与氧气发生反应变成黑色的氧化铜,且易发生爆炸;
故填:反应结束后先停止通氢气后撤酒精灯,导致生成的铜在余热的作用下又变成氧化铜;
⑤氢气无毒,而一氧化碳有毒不能直接排放到空气中,而该装置无尾气处理装置;
故填:因为一氧化碳有毒,反应没有在密封装置中进行同时没有尾气吸收;
⑥实验室常用氯酸钾在加热的情况下制取氧气,其反应方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;氧气能使带火星的木条复燃,验满时应将带火星的木条放在集气瓶口部,木条复燃,说明已满.
故填:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;带火星木条放在瓶口,看是否复燃.
点评 本题考查了氢气、一氧化碳还原氧化铜原理、实验中的注意点如尾气处理等.书写化学方程式时要遵循质量守恒定律.


 新思维寒假作业系列答案
新思维寒假作业系列答案科目:初中化学 来源: 题型:解答题
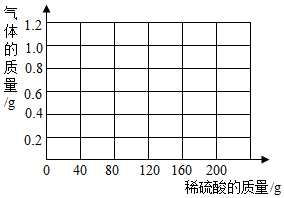 镁带在空气中放置一段时间表面会氧化,其中所含的其它杂质与稀硫酸不反应.为了测定某种镁带中镁的质量分数,某实验小组进行如下实验:先用细砂纸打磨镁带表面,使用精密天平称取打磨后11.25克镁带样品放在烧杯中,每次加入40.00克稀硫酸(不考虑水的挥发)使充分反应,测量反应前后装置连同内盛物质的质量.
镁带在空气中放置一段时间表面会氧化,其中所含的其它杂质与稀硫酸不反应.为了测定某种镁带中镁的质量分数,某实验小组进行如下实验:先用细砂纸打磨镁带表面,使用精密天平称取打磨后11.25克镁带样品放在烧杯中,每次加入40.00克稀硫酸(不考虑水的挥发)使充分反应,测量反应前后装置连同内盛物质的质量.| 加入稀硫酸次数 | 1 | 2 | 3 | 4 | 5 | 6 |
| 烧杯和所称物质总质量(克) | 120.15 | 159.95 | 199.75 | 239.55 | 279.45 | 319.45 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
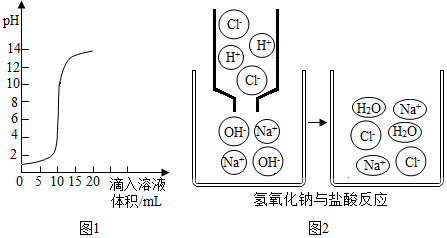
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
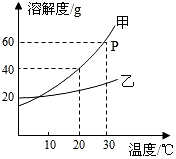 如图是甲、乙两种固体物质的溶解度曲线.据图回答:
如图是甲、乙两种固体物质的溶解度曲线.据图回答:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com