
废旧电路板中主要含有塑料、铜和锡(Sn)等,为实现对其中锡的绿色回收,某工艺流程如下。
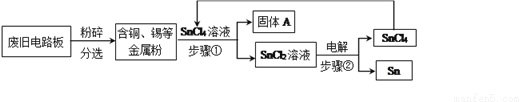
已知:Sn+SnCl4=2SnCl2
(1)SnCl4中锡元素的化合价是_____________________。
(2)铜的金属活动性比锡的________(填“强”或“弱”),固体A中一定含有的金属元素是_______。
(3)写出步骤②发生反应的化学方程式________________________________________。
(4)相比于直接焚烧废旧电路板回收金属,该工艺主要优点是__________________(回答一点即可)。
+4 弱 Cu 2SnCl2Sn+SnCl4 避免焚烧塑料产生污染,更加环保 【解析】(1)SnCl4中氯元素的化合价为-1价,根据化合价的代数和为0,锡元素的化合价是+4价; (2)铜的金属活动性比锡的弱;铜没有参加反应,故固体A中一定含有的金属元素是铜; (3)SnCl2溶液在通电的条件下反应生成Sn和SnCl4,反应方程式为2SnCl2Sn+SnCl4; (4)该工艺...科目:初中化学 来源:河南省2018届九年级招生模拟考试化学试卷 题型:单选题
以科学原理和实验事实为依据进行推理是学习化学的一种重要方法。下列推理得出的相关结论正确的是
A. 金刚石与石墨都是由碳元素组成的单质,所以它们的性质完全相同
B. 氢氧化钠固体加入水中温度升高是因为其溶于水放热,生石灰加入水中温度升高也因为氧化钙溶于水放热
C. 铁丝在氧气中能够燃烧,空气中有氧气,所以铁丝在空气中能够燃烧
D. 水通电能够生成氢气和氧气,说明水是由氢氧两种元素组成的
D 【解析】A、碳元素有金钢石、石墨、无定形碳等同素异形体。同素异形体由于结构不同,即原子排列不同,彼此间物理性质有差异;但由于是同种元素形成的单质,所以化学性质相似,错误;B、氢氧化钠固体加入水中温度升高是因为其溶于水放热,生石灰加入水中温度升高是因为氧化钙与水反应放热,错误;C、铁丝在氧气中能够燃烧,由于空气中氧气浓度低,铁丝在空气中不能燃烧,错误;D、水通电能够生成氢气和氧气,说明水是...查看答案和解析>>
科目:初中化学 来源:河北省2018年中考化学试卷 题型:推断题
A→L是初中化学常见物质,它们之间的转化关系如图所示。(反应条件已略去)。其中G是大理石的主要成分,A和I为红色固体,B、D和L为气体。
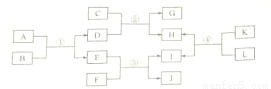
请回答下列问题:
(1)G的化学式为_____________。
(2)E的组成元素在化合物中常呈现的化合价有______。
(3)反应③的化学方程式为_____________。
(4)上述转化中,B和L表现出相应的化学性质是_______。
CaCO3 +2,+3 Fe+CuSO4=FeSO4+Cu或CuCl2+Fe=FeCl2+Cu或Fe+Cu(NO3)2=Fe(NO3)2+Cu 还原性 【解析】本题是框图型推断题。在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可。 G是大理石的主要成分,则G为CaCO3;A为红色固体,B、D为气体...查看答案和解析>>
科目:初中化学 来源:山东省济南市2018届九年级初中中考作业练习化学试卷 题型:科学探究题
某化学兴趣小组的同学无意中向2m L10%的氯化钙溶液中滴加氢氧化钠溶液,出现了白色沉淀。
【提出问题】观察到白色沉淀的原因是什么?
【猜想假设】
(1)氢氧化钠溶液变质,产生的白色沉淀是_________;
(2)氢氧化钠溶液浓度较大,产生的白色沉淀是氢氧化钙。
【实验探究】甲组同学针对猜想(1)进行实验。
实验步骤 | 实验现象 | 实验结论 |
将浑浊液过滤,取少量滤渣于烧杯中,加入足量水 | ________________________ | 猜想(1)不成立 |
乙组同学提出在甲组实验的基础上,从研究滤液的角度也可以证明氢氧化钙的存在,他们将滤液进行加热,观察到________________________,从而验证了自己的设想。
CaCO3 沉淀完全溶解 有白色浑浊产生 【解析】(1)氢氧化钠变质后生成的是碳酸钠,碳酸钠遇到氯化钙后生成碳酸钙沉淀; (2)碳酸钙是难溶于水的,结论1是不成立的,故沉淀不可能是碳酸钙,故沉淀是氢氧化钙,故加入足量 的水氢氧化钙完全溶解;氢氧化钙的溶解度随温度的升高而降低,故试管温度后,如有白色固体析出,说明有氢氧化钙;查看答案和解析>>
科目:初中化学 来源:山东省济南市2018届九年级初中中考作业练习化学试卷 题型:科学探究题
.钙元素是人体中重要的微量元素,钙元素组成的化合物种类有很多。 某实验探究小组想研究一些含钙化合物的性质:
(1)氧化钙溶于水制得熟石灰,该反应过程中能量的变化是_____填“吸热”或“放热”),氧化钙常用作______剂。
(2)氢化钙(CaH2)固体是登山运动员常用的能源提供剂,小明将一定量稀盐 酸滴入盛有氢化钙固体的锥形瓶中立刻观察到有大量气泡冒出,一段时间后变成 澄清的溶液。
【提出问题】①生成的气体是什么?
②澄清溶液中溶质的成分是什么?
【查阅资料】①氢化钙是一种灰白色固体,CaH2能与水反应生成Ca(OH)2和 一种可燃性气体。
②CaCl2溶液显中性
【猜想气体】小张认为气体为 CO,小明立刻否定。你认为他的理由是________;请你写出CaH2与水反应的化学方程式___________________;
【猜想溶质】猜想一:只有CaCl2猜想二:有________________(填化学式)
猜想三:有CaCl2和Ca(OH)2
【实验探究】为了验证猜想二,他们分别进行了下列三组实验
实验①:取少量溶液置于试管中,滴加紫色石蕊试液,观察到溶液颜色变成_____色,则猜想二正确
实验②:取少量溶液置于试管中,加入_______,观察到有气泡冒出,则猜想二 正确。
实验③:取少量溶液置于试管中,加入 CuO 粉末,观察到_______,则猜想二正确。
【得出结论】通过上述三组实验的探究,两位同学一致确定猜想二正确。
【评价反思】在分析反应后所得溶液中溶质的成分时,除考虑生成物外,还需要 考虑_______。
放热 干燥 反应物中不含有碳元素,不能生成一氧化碳 CaH2+2H2O=Ca(OH)2+2H2↑ CaCl2和HCl 红 活泼金属或碳酸盐 粉末溶解,溶液由无色变为蓝色 反应物是否有剩余 【解析】(1)氧化钙溶于水制得熟石灰,该反应过程中能量的变化是放热,因此氧化钙常用作干燥剂;(2)【猜想气体】小张认为气体为CO,小明立刻否定,他的理由是反应物中不含有碳元素,不能生成一氧化碳;氢化钙和...查看答案和解析>>
科目:初中化学 来源:安徽省2018年中考化学 题型:单选题
为实现二氧化碳的绿色利用,科学家用固碳酶作催化剂设计了如下转化过程。下列有关说法正确的是

A. 反应①的化学方程式为CO2+C=CO B. 固碳酶在反应前后化学性质发生变化
C. X的化学式为CH2 D. 该过程实现了无机物向有机物的转化
D 【解析】A、该反应方程式缺少条件,故错误; B、固碳酶是催化剂,故反应前后的质量和化学性质不变,故错误; C、由图可知,X的化学式为C2H4,故错误; D、该过程实现了无机物向有机物的转化,正确。故选D。查看答案和解析>>
科目:初中化学 来源:山东省青岛市2018年中考化学试卷 题型:推断题
同学们到实验室去进行“探究金属的性质”实验。将锌粉和铁粉的混合物加入到盛有一定量硝酸银溶液的烧杯中,充分反应后过滤,得到滤渣和滤液。请你填空。
(1)若将所得滤渣放入稀盐酸中,有气泡产生,则
①滤液里一定含有_____(填写化学式,下同),可能含有_____;
②滤渣中一定含有_____,可能含有_____。
(2)若反应后所得滤液呈无色,则滤渣中一定含有_____(填写化学式)。
(3)反应后所得滤液的溶质质量分数_____(选填“大于”、“等于”或“小于”)原硝酸银溶液的溶质质量分数。
Zn(NO3)2 Fe(NO3)2 Ag、Fe Zn Ag、Fe 小于 【解析】 由于金属的活动性是:锌比铁活泼,铁比银活泼,将锌粉和铁粉的混合物加入到盛有一定量硝酸银溶液的烧杯中,锌先和硝酸银反应生成硝酸锌和银,如果锌不足,则铁再和硝酸银反应生成硝酸亚铁和银。(1)若将所得滤渣放入稀盐酸中,有气泡产生,则说明滤渣中一定有铁,可能含有锌,溶液中的硝酸银完全参加了反应。①滤液里一定含有Z...查看答案和解析>>
科目:初中化学 来源:山东省青岛市2018年中考化学试卷 题型:单选题
根据你的化学知识和生活经验判断,下列说法错误的是
A. 打开浓盐酸试剂瓶瓶塞,能闻到刺激性气味,是因为分子在不断地运动
B. 滴加洗涤剂能将餐具上的油污洗掉,因为洗涤剂能溶解油污
C. 吃松花蛋时可加入少量食醋,因为食醋能消除蛋中所含碱性物质的涩味
D. 稀盐酸能用来除去铁制品表面的铁锈,因为稀盐酸能与某些金属氧化物反应
B 【解析】A、打开浓盐酸试剂瓶瓶塞,能闻到刺激性气味,是因为氯化氢分子是在不断的运动的,正确;B、滴加洗涤剂能将餐具上的油污洗掉,是因为洗涤剂有乳化作用,能将大的油珠分散成细小的油滴随水冲走,错误;C、吃松花蛋时可加入少量食醋,因为食醋能与蛋中所含碱性物质发生反应,能消除蛋中所含碱性物质的涩味,正确;D、稀盐酸能用来除去铁制品表面的铁锈,是因为酸能与金属氧化物反应,正确。故选B。 ...查看答案和解析>>
科目:初中化学 来源:湖北省黄冈市2018年中考化学试卷 题型:填空题
化学基础与常识
(1)下图金属应用的实例,主要利用金属的导热性的是_______(填序号);

A电缆 B.电热壶 C.金属丝 D.金属乐器
(2)向氢氧化钠溶液中滴加稀盐酸至恰好完全反应,反应前后溶液中存在的离子种类如图所示(其中“○”“ ”“●”“
”“●”“  ”表示不同离子)。则“○”与“
”表示不同离子)。则“○”与“ ”反应生成了_________(填物质名称)。
”反应生成了_________(填物质名称)。
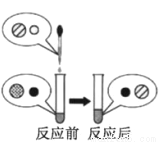
(3)氢氟酸(HF)能刻画玻璃,其中有一个化学反应的化学方程式是: CaSiO3+6HF=X+SiF4↑+3H2O,则X的化学式为_______________
(4)氢能是一种极具发展潜力的清洁能。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如图所示。
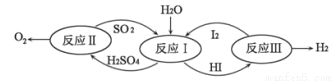
写出反应I中,发生反应的化学方程式:_____________________________。
B 水 CaF2 SO2+I2+2H2O=H2SO4+2HI 【解析】(1) A、电缆是利用金属的导电性,故错误;B、电热壶利用金属的导热性,故正确;C、金属丝利用金属的延展性,故错误;D、金属乐器利用金属具有金属光泽、硬度大,故错误;(2) 氢氧化钠与稀盐酸反应生成氯化钠和水,中和反应的实质是氢离子和氢氧根离子结合生成水分子;(3)在化学反应CaSiO3+6HF=X+SiF4↑+3H2O中...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com