
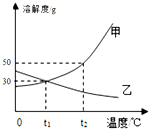
 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线.分析 (1)据配制溶液所用仪器分析解答;
(2)据该温度下二者的溶解度大小分析解答;
(3)不饱和溶液变为饱和溶液的一般方法有加入溶质、蒸发溶剂、降温,并结合选项解答;
(4)甲在t1℃的溶解度是30g,据此分析解答.
解答 解:(1)通常情况下,在实验室用固体甲配制一定溶质质量分数的甲溶液,需用到的仪器有:托盘天平(带砝码盒)、烧杯和药匙、玻璃棒、量取水的量筒、及定容的胶头滴管;
(2)t2℃时甲的 溶解度大于乙的溶解度,即等量的水中溶解甲的质量大于乙,所以将等质量的甲、乙两种物质加水溶解配制成饱和溶液,甲需要的水的质量少,则形成的溶液质量小;
(3)把甲物质的不饱和溶液变为饱和溶液,可采取加入溶质、蒸发溶剂、降温的方法;
A.若采取加入溶质和降温至恰好饱和的方法,则溶剂质量不变,故溶剂的质量一定变小是错误的;
B.若采取蒸发溶剂和降温至恰好饱和的方法,则溶质的质量不变,若采取加入溶质的方法,则溶质的质量不变,故溶质质量可能不变正确;
C.若采取降温至恰好饱和的方法,则溶质、溶剂的质量不变,溶质的质量分数不变,所以溶质的质量分数一定变大错误;
D.若采取降温至恰好饱和的方法,则溶质、溶剂的质量不变,溶液的质量不变,所以溶液的质量一定变大错误;
E.该饱和溶液是此温度下甲的饱和溶液,是其他物质的不饱和溶液,所以还可以溶解其他物质,正确;
(4)甲在t1℃的溶解度是30g,即该温度下100g水中最多溶解30g的甲,所以t2℃时,50g甲加入100g水中充分溶解后,降温到t1℃要析出20g的甲,所得溶液的溶质质量分数是$\frac{30g}{130g}$×100%≈23.1%;
故答案为:(1)BCFG; (2)<;(3)BE; (4)23.1%.
点评 明确溶解度概念的意义、溶解度曲线的意义、饱和溶液和不饱和溶液的相互转化方法,才能结合题意灵活分析解答.


 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案科目:初中化学 来源: 题型:选择题
| A. | Z的化学式为XY3 | |
| B. | 若mgX2和ngY2恰好完全反应,则生成(m+n)gZ | |
| C. | 若X2和Y2的相对分子质量分别为M和N,则Z的相对分子质量为(M+N) | |
| D. | 若ag X2完全反应生成bg Z,则同时消耗(b-a) g Y2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液. | 固体溶解时试管外壁发烫,试管底部有不容物,溶液变红. | 固体中一定含有CaO 多余和氢氧化钙. |
| (2)另取少量固体放于试管中,滴加足量的稀HCl. | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液. | 固体中一定含有Fe,一定不含Fe2O3 |
| (3)将步骤(2)中产生的气体通入到澄清的石灰水中 | 澄清石灰水变浑浊 | 固体中一定含有CaCO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
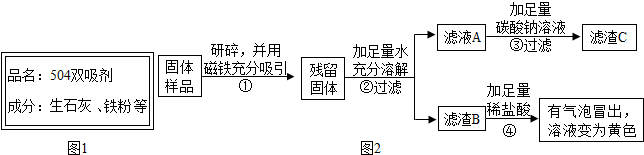
 “双吸剂”是常用的袋装食品的保鲜剂,可用来吸收氧气、二氧化碳、水蒸气等气体.某化学小组的同学在袋装食品中发现一包名为“504双吸剂”的保鲜剂,其标签如图所示.同学们对这包久置的“504双吸剂”的固体样品很好奇,设计实验进行探究.
“双吸剂”是常用的袋装食品的保鲜剂,可用来吸收氧气、二氧化碳、水蒸气等气体.某化学小组的同学在袋装食品中发现一包名为“504双吸剂”的保鲜剂,其标签如图所示.同学们对这包久置的“504双吸剂”的固体样品很好奇,设计实验进行探究.| 实验操作 | 实验现象 | 实验结论 |
| 一、取少量固体加入足量蒸馏水,搅拌溶解 | 固体部分溶解,并放出大量热 | 固体中一定含有CaO |
| 二、过滤,取滤液滴加无色酚酞试液 | 溶液变红色 | 固体中一定含有氢氧化钙 |
| 三、取滤渣加入足量稀盐酸 | 固体逐渐消失,产生大量无色气体,得到浅绿色溶液 | 固体中一定含有铁粉,一定不含有Fe2O3 |
| 四、将操作三中产生的气体通入到澄清石灰水中 | 澄清石灰水变浑浊 | 固体中一定含有CaCO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  | B. | 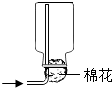 | ||
| C. | 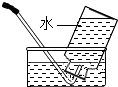 | D. | 选方法A或方法C都行 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com