
 如图是配制好的稀盐酸的标签,请根据标签上的文字信息,进行计算:
如图是配制好的稀盐酸的标签,请根据标签上的文字信息,进行计算:分析 根据碳酸钠和盐酸反应的化学方程式,已知二氧化碳的质量为4.4g,可求出参加反应的碳酸钠的质量和氯化氢的质量.从而求出纯碱样品中碳酸钠的质量分数.
解答 解:设碳酸钠的质量为x,消耗掉的盐酸溶液的质量为y
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 73 44
x y×10% 4.4g
$\frac{106}{x}=\frac{73}{y×10%}=\frac{44}{4.4g}$
x=10.6g;y=73g
纯碱样品中碳酸钠的质量分数为$\frac{10.6g}{11g}$×100%=96.4%
答:(1)纯碱样品中碳酸钠的质量分数为96.4%;
(2)用去稀盐酸的质量为73 g.
点评 本题难度不是很大,掌握利用化学方程式进行计算的方法是正确解答本题的关键.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 提倡使用太阳能电池等绿色环保电池 | |
| B. | 将废旧电池深埋,避免重金属污染 | |
| C. | 尽可能少使用一次性的纸杯、餐具 | |
| D. | 使用微生物降解塑料和光降解塑料,减少“白色污染” |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
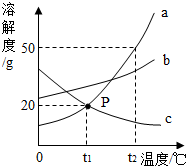 如图所示是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点,据图回答:
如图所示是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点,据图回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com