
 2Fe+3CO2
2Fe+3CO2 2Fe+3CO2
2Fe+3CO2

 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源:不详 题型:单选题
| A.水通电分解时生成氢气和氧气,说明水是由氢气和氧气组成 |
| B.通过在显微镜下观察木炭,得知木炭具有疏松多孔的结构 |
| C.天然气能在氧气中燃烧,说明氧气具有可燃性 |
| D.将石蕊试液滴入稀硫酸中溶液显红色,说明石蕊试液能使酸变红 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 实 验 步 骤 | 可能出现的实验现象 | 实验结论 |
| (1)取少量滤液于试管中,加入碳酸钠溶液 | 产生 | 假设③成立 |
| (2)取少量滤液于试管中,加入足量稀盐酸 | 放出无色气体 | 假设 成立 |
| (3)取少量滤液于试管中,加入碳酸钠溶液或足量稀盐酸 | 没有明显现象 | 假设 成立 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
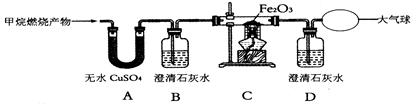
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
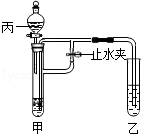
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
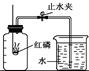
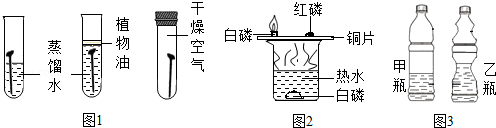
| | 颜色、状态 | 熔点/℃ | 着火点/℃ | 密度/(g/cm3) |
| 红磷 | 暗红色固体 | 590 | 240 | 2.34 |
| 白磷 | 白色或黄色固体 | 44.1 | 40 | 1.82 |
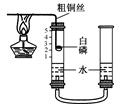
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 序号 | KClO3的质量 | 其他物质的质量 | 温度 | 氧气的体积 | 反应所需时间 |
| ① | 2.0g | | 330℃ | 100mL | T1 |
| ② | 2.0g | CuO 0.5g | 330℃ | 100mL | T2 |
| ③ | 2.0g | MnO2 0.5g | 330℃ | 100mL | T3 |
| ④ | 2.0g | MnO2 g | 380℃ | 100mL | T4 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 方案 | 步骤 | 现象 | 结论 |
| Ⅰ | ①取样品,滴加BaCl2溶液 ②对步骤①反应后的混合物进行过滤,在滤渣中滴加稀盐酸 | ①有白色沉淀产生 ②无明显现象 | 废液中含有SO42﹣ |
| Ⅱ | ①取样品,滴加过量_____________ ②在步骤①的溶液中滴加BaCl2溶液 | ①无明显现象 ②有白色沉淀产生 | 废液中含有SO42- |
| Ⅲ | ①取样品,滴加Ba(NO3)2溶液 ②对步骤①产生的混合物进行过滤,在滤渣中滴加稀硝酸 | ①有白色沉淀产生 ②无明显现象 | 废液中含有SO42- |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
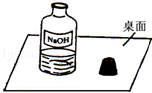
| 实验步骤 | 预期现象及结论 |
| | |
| | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com