
分析 本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.
解答 解:(1)原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.所以2个磷原子,就可表示为:2P;
(2)离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.故4个氧离子可表示为4O2-;
(3)根据分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,因此3个水分子表示为:3H2O;
(4)元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,所以正三价的铝离子,故可表示为:$\stackrel{+3}{Al}$;
(5)四氧化三铁的化学式为:Fe3O4;
(6)氮元素的符号为:N;
故答案为:(1)2P;(2)4O2-;(3)3H2O;(4)$\stackrel{+3}{Al}$;(5)Fe3O4;(6)N;
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
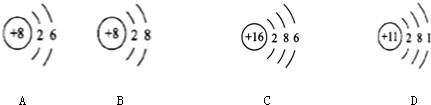
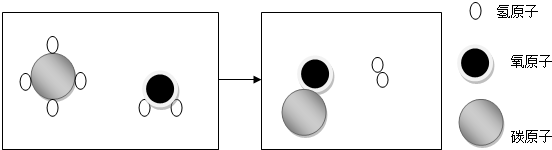
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
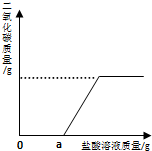 一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程
一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程| 样品质量 | 反应前总质量 | 反应后总质量 |
| 10.6克 | 148.5克 | 146.3克 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
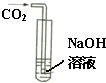 化学学习小组的同学们在探究氢氧化钠的性质时,将二氧化碳气体通入盛有氢氧化钠溶液的大试管中,如图所示,结果同学们没有观察到明显现象,于是他们展开了如下探究:
化学学习小组的同学们在探究氢氧化钠的性质时,将二氧化碳气体通入盛有氢氧化钠溶液的大试管中,如图所示,结果同学们没有观察到明显现象,于是他们展开了如下探究:| 实验操作 | 实验现象 | 结论 |
| ①取一定量大试管中的溶液于试管中,滴加过量CaCl2溶液,过滤. ②向滤液中滴加酚酞 | 溶液变成红色 | 贝贝的猜想成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 热敷袋中的活性炭会达到着火点而燃烧 | |
| B. | 热敷袋主要利用铁生锈放热 | |
| C. | 发热剂需接触空气才会发热 | |
| D. | 食盐能加快热敷袋中铁生锈的速度 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
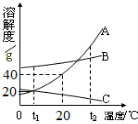 如图为A、B、C三种物质的溶解度曲线,据图回答:
如图为A、B、C三种物质的溶解度曲线,据图回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 化学与生活息息相关.
化学与生活息息相关.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com