
分析 (1)盐酸是由氢离子和氯离子构成的,硫酸是由氢离子和硫酸根离子构成的,据此进行分析解答;
(2)根据浓盐酸具有挥发性、浓硫酸具有吸水性进行分析解答;
(3)铁锈的主要成分是氧化铁,能和稀硫酸反应生成硫酸铁和水;
(4)根据酸的化学性质分析.
解答 解:(1)硫酸和盐酸都属于酸,硫酸和盐酸都属于酸,两者的不同主要是酸根的不同,从组成上看,两者的不同点是酸根离子不同;
故填:酸根离子;
(2)浓盐酸具有挥发性,打开盛有浓盐酸的试剂瓶,挥发出来的氯化氢气体遇到空气中的水蒸气形成盐酸小液滴,故瓶口上方出现白雾;而浓硫酸具有吸水性,打开盛有浓硫酸酸的试剂瓶,瓶口上方无明显变化;
故填:浓盐酸;
(3)生锈的铁钉插入足量的稀硫酸中,铁锈与盐酸反应,生成硫酸铁与水,化学方程式为:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;
故填:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;
(4)把硫酸转变成盐酸,即把硫酸中的硫酸根离子转变成氯离子,也就是把硫酸根离子转化成沉淀,因此应加入适量的氯化钡溶液,方程式为:H2SO4+BaCl2═BaSO4↓+2HCl;
故填:H2SO4+BaCl2═BaSO4↓+2HCl.
点评 本题难度不是很大,主要考查了酸的有关的化学性质,从而培养学生对知识的灵活运用的能力.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:推断题
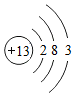 ;B离子
;B离子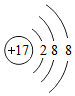 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com