
【题目】金属材料和水在生产和生活中有着广泛应用。
① 水是很好的溶剂。下表是 NaCl 和 KNO3 在不同温度时的溶解度,回答问题。
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度 | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
(g/100g 水) | KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 |
I.两种物质中,溶解度受温度影响变化较大的是______;
II.60℃时,按图示操作

A 中溶液是_______(填“饱和”或“不饱和”)溶液,C 中溶液的总质量是_______g;
III.50℃时,将两种物质的饱和溶液各 100 g,分别加热蒸发 10 g 水后,再恢复到 50℃, 则以下说法正确的是______(选填编号)。
a.有 NaCl 晶体析出,无 KNO3 晶体析出
b.两溶液中溶质与溶剂的质量比都增大
c.剩余溶液的质量:NaCl 溶液大于 KNO3 溶液 d.析出 NaCl 晶体 3.7 g
② 铁制品在潮湿空气中容易生锈,请写出工业上除铁锈的方法_________(用化学方程式表示)。
③ 某同学将一定质量的 Zn 粉放入 AgNO3 与 Cu(NO3)2 的混合溶液中,实验流程如图所示:
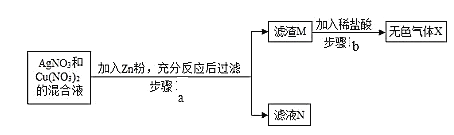
I.步骤 b 中生成的无色气体 X 是_________,滤液 N 中的溶质是_____;
II.步骤 a 中发生反应的化学方程式____(任写一个即可)。
【答案】 KNO3 不饱和 167.6 cd Fe2O3+6HCl=2FeCl3+3H2O H2 Zn(NO3)2 Zn+2AgNO3=2Ag+Zn(NO3)2或 Zn+Cu(NO3)2=Cu+Zn(NO3)2
【解析】① I、分析根据溶解度表可知,两种物质中溶解度受温度影响变化较大的是KNO3;
II、60℃时,KNO3的溶解度是110.0g,即60℃时,100g水中溶解110.0g KNO3达到饱和状态,A中溶液有水100g ,KNO340g,所以A中溶液是不饱和溶液;20℃时,KNO3的溶解度是31.6g,即20℃时,100g水中最多溶解31.6g KNO3,20℃时,NaCl的溶解度是36g,即20℃时,100g水中最多溶解36gNaCl,C 中溶液的总质量=100g+36g+31.6g=167.6g;
III、a、50℃时,将两种物质的饱和溶液各 100 g,分别加热蒸发 10 g 水后,再恢复到 50℃,都有晶体析出,错误; b、50℃时,将两种物质的饱和溶液各 100 g,分别加热蒸发 10 g 水后,再恢复到 50℃,两溶液仍为饱和溶液,两溶液中溶质与溶剂的质量比没有改变,错误; c、由表中的数据可知,在50℃时,KNO3溶解度大于NaCl的溶解度,所以50℃时,将两种物质的饱和溶液各100g,分别加热蒸发10g水后,再恢复到50℃,KNO3析出的晶体多,剩余溶液的质量:NaCl溶液大于KNO3溶液,正确; d、设:析出 NaCl 晶体质量为x,则有100g:37g=10g:x,x=3.7g,正确。故选cd;
②工业上除铁锈的方法是用稀盐酸与氧化铁反应生成氯化铁和水,化学方程式是:Fe2O3+6HCl=2FeCl3+3H2O;
③由于金属的活动性是:锌>铜>银,将一定质量的Zn粉放入AgNO3与Cu(NO3)2的混合溶液中,锌先与硝酸银反应生成了银和硝酸锌,当硝酸银完全反应后,再与硝酸铜反应生成了硝酸锌和铜。由流程图可知,向过滤后的滤渣中加稀硫酸有气泡生成,说明了锌粉是过量的,生成的无色气体应为氢气,溶液中的硝酸银和硝酸铜完全发生了反应,所以:
(1)步骤Ⅱ中生成的无色气体X是氢气,该反应锌与稀硫酸反应生成了硫酸锌和氢气,基本反应类型是置换反应,滤液N中的溶质是硝酸锌;
(2)由上述分析可知,步骤Ⅰ中所发生的反应的化学方程式有:Zn+2AgNO3═Zn(NO3)2+2Ag、Zn+Cu(NO3)2═Zn(NO3)2+Cu。


科目:初中化学 来源: 题型:
【题目】实验室常用下列装置制取有关气体。

(1)写出标有序号的一种仪器的名称_____________________。
(2)装置B除了用于制取氧气外,还可用来制取的气体是__________(写一种即可)。
(3)C装置可用来测量生成的CO2气体的体积,其中在水面上放一层植物油的目的是____________。
(4)上述两种方法都能用于实验室制取氧气。从制备气体的角度分析,你认为用其中相对较好的方法制取氧气时,选用的装置是____________,理由是__________________。
(5)实验室常用氯化铵固体与碱石灰固体共热来制取氨气。常温下氨气是一种无色、有刺激性气味的气体,密度比空气小,氨气极易溶于水。制取氨气反应的文字表达式:氯化铵+熟石灰![]() 氯化钙+氨气+水。若要用装置A制取氨气,该装置中存在的一处错误是________________。小红用湿润的红色石蕊试纸来检验NH3,产生的现象是______________________。
氯化钙+氨气+水。若要用装置A制取氨气,该装置中存在的一处错误是________________。小红用湿润的红色石蕊试纸来检验NH3,产生的现象是______________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组同学称取10g氧化铜和碳粉,通过下列实验对其中炭粉含量进行探究。实验前进行知识准备:2Cu + O2 ![]() 2CuO
2CuO
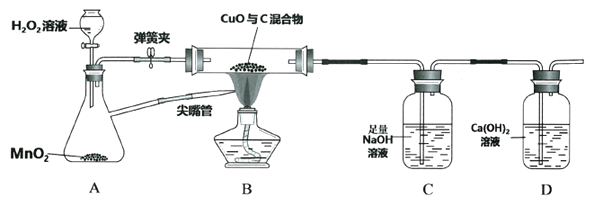
(1)关闭弹簧夹,打开分液漏斗活塞。写出A中的化学反应方程式________________________________。
(2)点燃酒精灯,将尖嘴管对着火焰,以提高温度,其原因是________________________________。玻璃管中发生的反应为 木炭还原氧化铜:C+ 2CuO → 2Cu + CO2↑,该反应条件是__________。
(3)反应一段时间,装置B中一定会观察到_____________________。装置D中澄清石灰水不变浑浊,说明__________________________________________。
(4)再打开弹簧夹,继续加热装置B,装置C中观察到的现象是____________________。
直至固体颜色不再变化后停止加热,称量装置C,质量比反应前增重4.4g,增重质量就是____________质量。通过计算可知装置B中含碳元素质量为____________g。本实验还可以通过称量____________________,也能计算出原混合物中碳的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国科学家研制出一种催化剂,能在室温下高效催化空气中一种有毒气体,其反应如下图:下列说法,正确的是( )

A. 该反应属于置换反应 B. 这种有毒气体的化学式为HCHO
C. 其中有三种物质属于氧化物 D. 该反应中A与C的质量比为1:1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种固体物质的溶解度曲线如下图所示,其中a、b、c三点的坐标分别为(42,63)、(67,38)、(67,25):
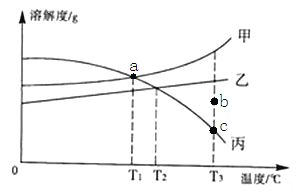
(1)T3℃时,三种固体物质的饱和溶液中溶质质量分数由小到大的顺序是___________;
(2)a点的意义为_________________________________________;
(3)对乙物质来说,b点所处的溶液状态为____________(填“饱和”或“不饱和”)溶液;
(4)要使T3℃时接近饱和的丙溶液变成该温度下的饱和溶液,可采用的一种方法是_____;
(5)T3℃时,若将125g丙物质的饱和溶液降温到T1℃,还能溶解固体丙的质量为________g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一包白色粉末可能由NaCl、NaNO3、MgCl2、CuSO4、中的一种或多种物质组成。小明为了探究其成分,设计并完成了如下图所示的实验。
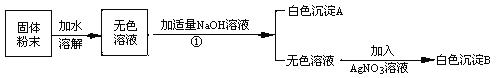
根据以上实验,回答:
操作①是
原固体粉末中一定没有的成分是
生成沉淀A的化学方程式是
根据上述实验 (填‘能’或‘不能’)确定原固体粉末中含有NaCl、NaNO3。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列化学反应前后,硫元素的化合价没有发生变化的是
A. S+O2 ![]() SO2
SO2
B. 2H2S+SO2=3S+2H2O
C. CuO+H2SO4=CuSO4+H2O
D. Cu+2 H2SO4(浓)![]() CuSO4 +2H2O+SO2↑
CuSO4 +2H2O+SO2↑
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】酸、碱、盐在生产生活中具有广泛的用途。
(1)制作“叶脉书签”需用到10%的氢氧化钠溶液。现配制100g质量分数为10%的氢氧化钠溶液。
①若用氢氧化钠固体配制,需称量氢氧化钠的质量为__________g。
②用氢氧化钠固体配制10%的氢氧化钠溶液过程中,需要用到的仪器除了托盘天平、药匙、烧杯、玻璃棒、胶头滴管、试剂瓶外,还需要__________。
③下列操作正确的是__________(填字母序号)。
A.称量氢氧化钠固体时,左盘放砝码
B.在托盘天平的左右托盘上垫滤纸称量氢氧化钠固体
C.将准确称量的氢氧化钠固体放入装有水的量筒中溶解
D.将配好的氢氧化钠溶液装入试剂瓶中,塞好瓶塞并贴上标签
④若用20%的氢氧化钠溶液加水(水的密度为1g/cm3)配制100g质量分数为10%的氢氧化钠溶液,需20%的氢氧化钠溶液的质量为_________g;配制时应选用_________mL的量筒取水(填“100”或“50”或10)。
(2)某固体粉末可能含有碳酸钙、硫酸钠、氯化钠、氯化钡、硫酸铜中的一种或几种。为确定该固体粉末的成分,进行了如下实验:

回答下列问题:
①反应Ⅰ的化学方程式为__________________________。
②白色沉淀C是_________________(填化学式)。
③原固体粉末中一定不含________________、______________(填化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2017年4月,科学家在深海海底发现了大量未来太阳能光伏发电必需的元素——碲,碲元素的相关信息如图所示。下列说法正确的是

A. 碲原子的质子数为52 B. 碲是金属元素
C. 碲原子的中子数为52 D. 碲元素的相对原子质量为127.6g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com