
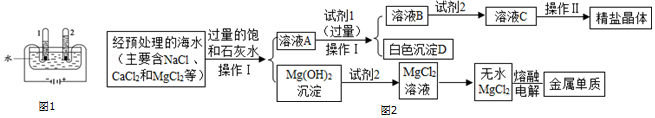
分析 (1)电解水时,正极产生的是氧气,负极产生的是氢气,氧气和氢气的体积比约为1:2;
(2)操作I是过滤,过滤所用到的仪器有铁架台、漏斗、烧杯、玻璃棒等;
试剂1是碳酸钠溶液,用来除去溶液中的氯化钙和过量的氢氧化钙;
玻璃棒用途有搅拌、引流、转移物质等;
在熔融状态下电解无水氯化镁生成镁和氯气;
(3)若用量筒量取水时俯视读数,会导致量取水的体积偏小,从而导致配制溶液质量分数偏大;
(4)氢氧化钠能和空气中的二氧化碳反应生成碳酸钠和水;
碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,根据反应的化学方程式及其提供的数据可以进行相关方面的计算.
解答 解:(1)通电一段时间后,试管1中所收集的气体较多,是氢气,氢气的化学式为H2.
故填:H2.
(2)①操作I是过滤,过滤所用到的仪器有铁架台、漏斗、烧杯、玻璃棒等.
故填:铁架台、漏斗、烧杯、玻璃棒等.
②试剂1是碳酸钠溶液,用来除去溶液中的氯化钙和过量的氢氧化钙.
故填:碳酸钠溶液.
③操作Ⅱ是蒸发,其中玻璃棒的作用是使液体均匀受热,防止液体飞溅.
故填:使液体均匀受热,防止液体飞溅.
④在熔融状态下电解无水氯化镁生成镁和氯气,反应的化学方程式为:MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑.
故填:MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑.
(3)某同学用蒸馏水配制一定质量分数的氢氧化钠溶液,若用量筒量取水时俯视读数,会导致量取水的体积偏小,则所配制溶液的溶质的质量分数偏大.
故填:偏大.
(4)①氢氧化钠敞口放置易变质,是因为氢氧化钠能和二氧化碳反应生成碳酸钠和水,反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O.
故填:2NaOH+CO2═Na2CO3+H2O.
②设碳酸钠质量为x,
Na2CO3+2HCl=2NaCl+H2O+CO2↑,
106 44
x 2.2g
$\frac{106}{x}$=$\frac{44}{2.2g}$,
x=5.3g,
样品中氢氧化钠的质量分数为:$\frac{50g-5.3g}{50g}$×100%=89.4%,
答:样品中氢氧化钠的质量分数为89.4%.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| 物 质 | 杂 质 | 试剂或方法 | |
| A | 氢氧化钠 | 氢氧化钙 | 加适量碳酸钠溶液后过滤 |
| B | 硫酸镁 | 硫酸铜 | 加镁粉后过滤 |
| C | 盐酸 | 硫酸 | 加适量氯化钡溶液后过滤 |
| D | 铁粉 | 铜粉 | 加硫酸铜溶液后过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
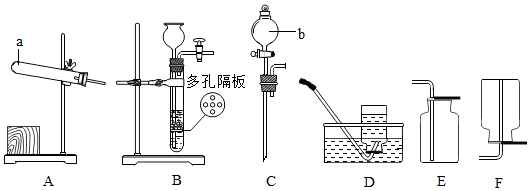
 根据如图所示二氧化碳和氧气的性质实验,请回答以下问题.
根据如图所示二氧化碳和氧气的性质实验,请回答以下问题.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
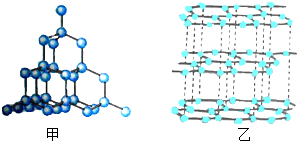 如图是甲、乙两种物质的结构示意图,图中小圆圈均代表碳原子.这两种物质在氧气中完全燃烧后的产物都是二氧化碳,但它们的物理性质却明显不同,如导电性、硬度等.据此,下列说法错误的是( )
如图是甲、乙两种物质的结构示意图,图中小圆圈均代表碳原子.这两种物质在氧气中完全燃烧后的产物都是二氧化碳,但它们的物理性质却明显不同,如导电性、硬度等.据此,下列说法错误的是( )| A. | 甲乙两种物质中的碳原子大小相同 | |
| B. | 将甲乙两种物质混合后得到的是纯净物 | |
| C. | 甲乙两种物质中原子的空间排列方式不同 | |
| D. | 甲乙两种物质由相同的原子构成 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
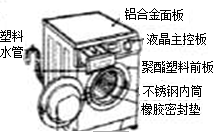 洗衣机是生活中家庭常用的必需品,如图所示是某品牌洗衣机图,请回答下列问题.
洗衣机是生活中家庭常用的必需品,如图所示是某品牌洗衣机图,请回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质(括号内为杂质) | 去除杂质的方法 |
| A | NaCl溶液(Na2CO3) | 加入过量的Ca(NO3)2溶液、过滤 |
| B | CaO(CaCO3) | 加水、过滤 |
| C | Cu(Fe) | 加过量H2SO4溶液、过滤 |
| D | HNO3溶液(H2SO4) | 加适量BaCl2溶液、过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com