
分析 (1)①据溶解时玻璃棒的作用解答;
②根据氯化钡与硫酸钠反应原理书写方程式;
③据碳酸钠可与氯化钡反应分析解答;
④据反应流程图分析滤液成分;加入稀盐酸是为了除去滤液中过量的碳酸钠,所以可据加入盐酸时溶液中是否有气泡产生,判断碳酸钠是否被除尽;
⑤蒸发时当蒸发皿中有较多固体出现时即可停止加热,用蒸发皿的余热蒸干;
(2)①根据溶质质量=溶液质量×溶质的质量分数,计算出所需氯化钠固体的质量,进而确定所选砝码的质量和游码的示数;
②溶剂质量=溶液质量-溶质质量,据此进行分析解答.
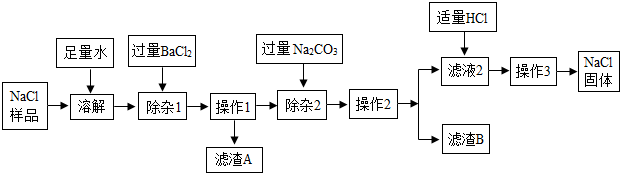
解答 解:(1)该实验流程是:加入水溶解形成硫酸钠、氯化钠的混合液,然后加入过量氯化钡除去硫酸钠,过滤得到滤液1,其成分是氯化钠、和过量的氯化钡,加入过量碳酸钠除去滤液中的氯化钡,过滤得到滤液2,其中含有生成的氯化钠和原来就有的氯化钠,及过量的碳酸钠,再加入适量的盐酸将过量的碳酸钠反应掉,得到氯化钠溶液,再加热蒸发即可得纯净的氯化钠固体;
①溶解中,向NaCl样品中加入足量水,用玻璃棒进行搅拌,目的是搅拌,加速固体.
②除杂1中,BaCl2溶液与杂质Na2SO4发生反应成硫酸钡沉淀和氯化钠,反应的化学方程式是BaCl2+Na2SO4=BaSO4↓+2NaCl.
③由上述分析可知:除杂2中,加入“过量Na2CO3”的目的是除去加入的过量的氯化钡,将钡离子形成沉淀反应掉,其离子符号是Ba2+;
④由上述分析可知:加入适量HCl前,滤液2中存在的溶质是过量的碳酸钠和氯化钠.在装有滤液2的烧杯中,加入适量HCl的操作方法是:向滤液中滴加适量稀盐酸,至恰好无气泡产生.
⑤操作3中,将滤液2放在蒸发皿中蒸发,当蒸发皿中 出现较多固体时,停止加热,用蒸发皿的余热蒸干.
(2)实验室现在要配制150g质量分数为16%的NaCl溶液.
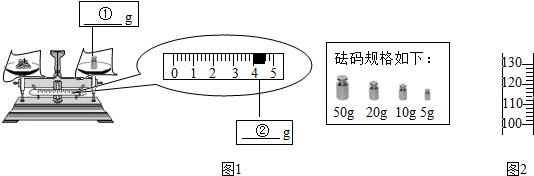
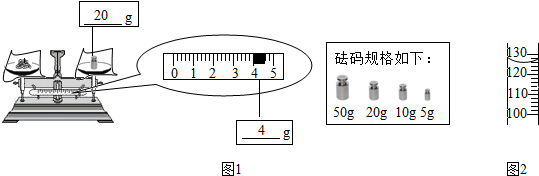
①溶质质量=溶液质量×溶质的质量分数,配制150g质量分数为16%的NaCl溶液,所需NaCl固体的质量为150g×16%=24g;选用20g的砝码,游码拨到4g处即可.见下图;
②需要水的质量是150g-24g=126g,即124mL,读数时视线与凹液面的最低处相平,见下图;
故答案为:(1)①搅拌,加速溶解;
②BaCl2+Na2SO4=BaSO4↓+2NaCl;
③Ba2+;
④NaCl、Na2CO3;向滤液中滴加适量稀盐酸,至恰好无气泡产生;
⑤出现较多固体;
(2)
点评 本题主要考了在粗盐提纯的试验中对杂质进行转换的探究,除去杂质的同时不能引入新的杂质,并明确溶质的质量分数计算等相关知识,综合性较强.


科目:初中化学 来源: 题型:实验探究题
| 20℃ | 8%Na2CO3溶液 | 8%NaHCO3溶液 |
| pH | 10.6 | 8.0 |
| 溶解度 | 10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
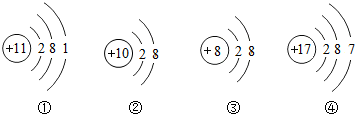
| A. | ①在化合物中的化合价通常为+1 价 | B. | ②的化学性质比较稳定 | ||
| C. | ③是一种阳离子 | D. | ④容易得到电子 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CuO+2HCl=CuCl2+H2O | B. | BaCl2+H2SO4=BaSO4↓+2HCl | ||
| C. | Ca(OH)2+2HNO3=Ca(NO3)2+2H2O | D. | 2NaOH+CO2=Na2CO3+H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 2Na+中“2”表示钠离子的个数是2 | |
| B. | H2中“2”表示每个氢分子中含有2个氢原子 | |
| C. | 2 H2表示2个氢分子 | |
| D. | Mg2+中的“2”表示镁元素的化合价为+2价 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com