
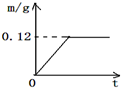
 小华想测定Cu-Zn合金和Cu-Ag合金中铜的质量分数,实验室只提供了一瓶稀盐酸和相关的仪器. (相关化学方程式:H2SO4+Zn═ZnSO4+H2↑)
小华想测定Cu-Zn合金和Cu-Ag合金中铜的质量分数,实验室只提供了一瓶稀盐酸和相关的仪器. (相关化学方程式:H2SO4+Zn═ZnSO4+H2↑)分析 在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,利用氢气的质量根据反应的反应方程式即可求得合金中排在氢前面金属的质量,进而求得铜的质量和其含量,据此分析解答即可.
解答 解:(1)Cu-Zn合金中的锌在氢的前面,能与盐酸反应生成氢气,而铜不与盐酸反应生成氢气,依据氢气的质量可求锌的质量,进而能测出铜的质量分数.
Cu-Ag中的金属都不与盐酸反应生成氢气,因此不能测出铜的质量分数.
(2)设参加反应的锌的质量为x
Zn+2HCl═ZnCl2+H2↑
65 2
x 0.12g
$\frac{65}{x}=\frac{2}{0.12g}$
x=3.9g
该合金中铜的质量分数为:$\frac{10g-3.9g}{10g}×$100%=61%;
(3)要求盐酸的溶质的质量分数,需知道溶质的质量和溶液的质量,知道所用的盐酸的体积和盐酸的密度,能求出盐酸的质量,而溶质的质量可以通过氢气的质量求出.
故答案为:(1)Cu-Zn;(2)该合金中铜的质量分数为61%;(3)B.
点评 本题考查了金属的性质以及根据化学方程式进行的计算,完成此题,可以依据已有的知识进行.


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:初中化学 来源: 题型:选择题
| A. | CO和CO2都能置动物死亡,所以它们都有毒 | |
| B. | 生铁和钢是含碳量不同的两种合金 | |
| C. | 合成药物的研发和发展、使用,保障了人体健康 | |
| D. | 不能用工业盐(NaNO2)烹饪食物 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 盐溶液 | NaCl | Na2CO3 | BaCl2 |
| pH | 等于7 | 大于7 | 等于7 |
| 实验步骤 | 实验现象 | 实验结论 |
| ①称取上述氢氧化钠固体样品8.0g溶于50mL,水配成溶液,向溶液中滴加氯化钡溶液至过量,充分反应后,静置. | 产生白色沉淀 | 说明久置固体中,一定含有 Na2CO3(填化学式). |
| ②用玻璃棒蘸取少量①中充分反应后的上层清液滴在一小块pH试纸上,与标准比色卡对比,测出pH | pH=11 | 说明久置固体中,还一定含有NaOH(填化学式). |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 硝酸钾的饱和溶液变为不饱和溶液,溶质质量分数一定变小 | |
| B. | 生成盐和水的反应一定是中和反应 | |
| C. | 酸中一定存在氢元素,碱中一定存在氢氧元素,盐中一定存在金属元素 | |
| D. | 加到双氧水里的二氧化锰在反应前后质量和化学性质一定不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com