

·ÖĪö £Ø1£©øßĪĀĢõ¼žĻĀ£¬Ģ¼ĖįøĘ·Ö½āÉś³ÉŃõ»ÆøĘŗĶ¶žŃõ»ÆĢ¼£¬Ģ¼ĖįĆ¾·Ö½āÉś³ÉŃõ»ÆĆ¾ŗĶ¶žŃõ»ÆĢ¼£»
¹żĀĖÄܹ»°Ń²»ČÜÓŚĖ®µÄ¹ĢĢå“ÓŅŗĢåÖŠ·ÖĄė³öĄ“£»
£Ø2£©Ńõ»ÆøĘŗĶĖ®·“Ӧɜ³ÉĒāŃõ»ÆøĘ£¬ĒāŃõ»ÆøĘŗĶĻõĖįļ§·“Ӧɜ³ÉĻõĖįøĘ”¢Ė®ŗĶ°±Ęų£»
£Ø3£©Alʬ±ķĆęµÄŃõ»ÆĤŹĒŃõ»ÆĀĮ£¬ÄÜŗĶĒāŃõ»ÆÄĘ·“Ӧɜ³ÉĘ«ĀĮĖįÄĘŗĶĖ®£»
£Ø4£©ĮņĖįļ§ŗĶĒāŃõ»ÆøĘ·“Ӧɜ³ÉĮņĖįøĘ”¢Ė®ŗĶ°±Ęų£»
£Ø5£©øł¾ŻĪļÖŹµÄ»ÆѧŹ½æÉŅŌ¼ĘĖć×é³ÉŌŖĖŲµÄÖŹĮæ·ÖŹż£®
½ā“š ½ā£ŗ£Ø1£©ģŃ·ŪÖ÷ŅŖŗ¬Ģ¼ĖįøĘ·Ö½ā²śÉśµÄŃõ»ÆøĘŗĶĢ¼ĖįĆ¾·Ö½ā²śÉśµÄŃõ»ÆĆ¾£»
²Ł×÷XĪŖ¹żĀĖ£®
¹ŹĢī£ŗŃõ»ÆøĘ”¢Ńõ»ÆĆ¾£»¹żĀĖ£®
£Ø2£©ÓĆŹŹĮæNH4NO3ČÜŅŗ½žČ”ģŃ·ŪŹ±£¬Ńõ»ÆøĘŗĶĖ®·“Ӧɜ³ÉĒāŃõ»ÆøĘ£¬ĒāŃõ»ÆøĘŗĶĻõĖįļ§·“Ӧɜ³ÉĻõĖįøĘ”¢Ė®ŗĶ°±Ęų£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗCaO+H2OØTCa£ØOH£©2£¬
2NH4NO3+Ca£ØOH£©2$\frac{\underline{\;\;”÷\;\;}}{\;}$Ca£ØNO3£©2+2H2O+2NH3”ü£®
¹ŹĢī£ŗCaO+H2OØTCa£ØOH£©2£»2NH4NO3+Ca£ØOH£©2$\frac{\underline{\;\;”÷\;\;}}{\;}$Ca£ØNO3£©2+2H2O+2NH3”ü£®
£Ø3£©Alʬ±ķĆęµÄŃõ»ÆĤŹĒŃõ»ÆĀĮ£¬ÄÜŗĶĒāŃõ»ÆÄĘ·“Ӧɜ³ÉĘ«ĀĮĖįÄĘŗĶĖ®£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗAl2O3+2NaOH=2NaAlO2+H2O£®
¹ŹĢī£ŗAl2O3+2NaOH=2NaAlO2+H2O£®
£Ø4£©øĆ¹¤ŅÕÖŠ²»ÄÜÓĆ£ØNH4£©2SO4“śĢęNH4NO3£¬ŌŅņŹĒĮņĖįļ§ŗĶĒāŃõ»ÆøĘ·“Ӧɜ³ÉµÄĮņĖįøĘĪ¢ČÜÓŚĖ®£¬»įµ¼ÖĀĢ¼ĖįøĘÖŠ»ģÓŠĮņĖįøĘ£®
¹ŹĢī£ŗĮņĖįļ§ŗĶĒāŃõ»ÆøĘ·“Ӧɜ³ÉµÄĮņĖįøĘĪ¢ČÜÓŚĖ®£¬»įµ¼ÖĀĢ¼ĖįøĘÖŠ»ģÓŠĮņĖįøĘ£®
£Ø5£©ĘßĀĮŹ®¶žøĘ£Ø12CaO•7A12O3£©ÖŠøĘŌŖĖŲµÄÖŹĮæ·ÖŹżĪŖ£ŗ$\frac{40”Į12}{56”Į12+102”Į7}$”Į100%=34.6%£¬
¹ŹĢī£ŗ34.6%£®
µćĘĄ ±¾ĢāÖ÷ŅŖæ¼²éĪļÖŹµÄŠŌÖŹ£¬½ā“šŹ±ŅŖøł¾Żø÷ÖÖĪļÖŹµÄŠŌÖŹ£¬½įŗĻø÷·½ĆęĢõ¼ž½ųŠŠ·ÖĪö”¢ÅŠ¶Ļ£¬“Ó¶ųµĆ³öÕżČ·µÄ½įĀŪ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
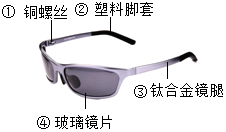 ŃŪ¾µŹĒČĖĆĒ³£ÓƵĻ¤ŃŪ¹¤¾ß£®ČēĶ¼ŹĒŅ»æī±äÉ«ŃŪ¾µµÄŹ¾ŅāĶ¼£ŗ
ŃŪ¾µŹĒČĖĆĒ³£ÓƵĻ¤ŃŪ¹¤¾ß£®ČēĶ¼ŹĒŅ»æī±äÉ«ŃŪ¾µµÄŹ¾ŅāĶ¼£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  ²ā¶ØæÕĘųÖŠŃõĘųµÄŗ¬Įæ | B£® |  ¼ÓČČŗó”¢ĪÅĘųĢåµÄĘųĪ¶ | ||
| C£® | 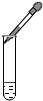 ĻņŹŌ¹ÜÖŠµĪ¼ÓŅŗĢå | D£® | 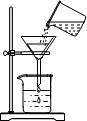 ¹żĀĖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢ½¾æĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢ½¾æĢā
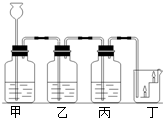 ČēĶ¼ŹĒijĶ¬Ń§Éč¼ĘµÄŹµŃé×°ÖĆ£¬ĒėÄć»Ų“šĻĀĮŠĪŹĢā£ŗ
ČēĶ¼ŹĒijĶ¬Ń§Éč¼ĘµÄŹµŃé×°ÖĆ£¬ĒėÄć»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µē½āĖ®£ŗ2H2O$\frac{\underline{\;Ķصē\;}}{\;}$2H2”ü+O2”ü | |
| B£® | ½¹ĢæÓėĖ®ÕōĘų·“Ó¦£ŗC+H2O$\frac{\underline{\;øßĪĀ\;}}{\;}$H2+CO | |
| C£® | Ģ«Ńō¹ā·Ö½āĖ®£ŗ2H2O$\frac{\underline{Ģ«ŃōÄÜ}}{“߻ƼĮ}$2H2”ü+O2”ü | |
| D£® | ĢģČ»ĘųÓėĖ®·“Ó¦£ŗCH4+H2O$\frac{\underline{\;øßĪĀ\;}}{\;}$CO+3H2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 »Æѧµē³ŲŹĒŅ»ĄąÖŲŅŖµÄÄÜŌ“£¬·Ļ¾Éµē³ŲÖŠµÄŠķ¶ąĪļÖŹŹĒæÉŅŌ»ŲŹÕĄūÓĆµÄ£®Ä³ÖÖŠĶŗŵÄøɵē³ŲµÄĘŹĆęĶ¼ČēĶ¼ĖłŹ¾£®ĻÖ¶ŌĘäÖŠµÄĢī³äĪļ£ØMnO2”¢C”¢æÉČÜŠŌĢī³äĪļ£©½ųŠŠĢ½¾æ£¬ĒėĢīæÕ£ŗ
»Æѧµē³ŲŹĒŅ»ĄąÖŲŅŖµÄÄÜŌ“£¬·Ļ¾Éµē³ŲÖŠµÄŠķ¶ąĪļÖŹŹĒæÉŅŌ»ŲŹÕĄūÓĆµÄ£®Ä³ÖÖŠĶŗŵÄøɵē³ŲµÄĘŹĆęĶ¼ČēĶ¼ĖłŹ¾£®ĻÖ¶ŌĘäÖŠµÄĢī³äĪļ£ØMnO2”¢C”¢æÉČÜŠŌĢī³äĪļ£©½ųŠŠĢ½¾æ£¬ĒėĢīæÕ£ŗ²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com