
| 实验操作 | 实验现象 | 实验结论及解释 | |
| ① | 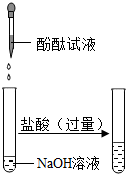 | 氢氧化钠可以与盐酸反应. 该反应的化学方程式为: NaOH+HCl═NaCl+H2O | |
| ② | 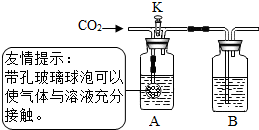 小军选用NaOH和Ca(OH)2两种溶液分别放入上边装置中的广口瓶中,关闭K,通入二氧化碳. | A、B中均无明显变化. | B中盛放的溶液是氢氧化钙溶液. 该实验目的是 检验二氧化碳能和氢氧化钠反应. |
分析 设计实验:
氢氧化钠溶液显碱性,能使酚酞试液变红色,能和稀盐酸反应生成氯化钠和水;
二氧化碳能使澄清石灰水变浑浊;
反思交流:
酚酞试液遇中性溶液和酸都不变色,遇碱性溶液变红色,故在氢氧化钠溶液中滴加酚酞试液变红,再加入盐酸至过量后,红色退去,要想证明酚酞试液又变无色是由于氢氧化钠与盐酸反应的结果,而不是过量的盐酸导致的,应加入适量的盐酸;
根据题意可知,此实验的目的是要验证氢氧化钠能与二氧化碳反应,故A中应加入氢氧化钠溶液,B中应加入氢氧化钙溶液,并通入大量二氧化碳气体,因为“通常状况下,1体积的水约能溶解1体积二氧化碳”,由于量取了40ml溶液放入A,若二氧化碳不与氢氧化钠反应,则A最多能溶解40ml二氧化碳,剩余的二氧化碳一定进入B,会使氢氧化钙溶液变浑浊,若二氧化碳与氢氧化钠溶液反应,就无剩余的二氧化碳再与氢氧化钙反应,所以“A、B中均无明显变化”,此实验可以说明二氧化碳和氢氧化钠发生了反应,其理由是关闭K时,B中溶液无明显变化,且通入的二氧化碳体积远大于A中溶液的体积,说明二氧化碳和氢氧化钠发生了反应.
解答 解:设计实验:氢氧化钠溶液显碱性,能使酚酞试液变红色,能和稀盐酸反应生成氯化钠和水;
二氧化碳能使澄清石灰水变浑浊,实验过程如下表所示:
| 实验操作 | 实验现象 | 实验结论及解释 | |
| ① |  | 溶液由红色变成无色 | 氢氧化钠可以与盐酸反应. 该反应的化学方程式为: NaOH+HCl═NaCl+H2O |
| ② |  小军选用NaOH和Ca(OH)2两种溶液分别放入上边装置中的广口瓶中,关闭K,通入二氧化碳. | A、B中均无明显变化. | B中盛放的溶液是氢氧化钙溶液. 该实验目的是检验二氧化碳能和氢氧化钠反应. |
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


科目:初中化学 来源: 题型:选择题
 关于水的电解实验,下列说法正确的是( )
关于水的电解实验,下列说法正确的是( )| A. | 这个实验证明了水是由氧气和氢气组成的 | |
| B. | 电解水生成的氢气和氧气质量比为2:1 | |
| C. | 水电解是化学变化 | |
| D. | 实验证明水是一种混合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 胃泰xxx |
| 抑酸剂 |
| 用量:每次2片,每天3次 |
| 有效成分:氢氧化铝 |
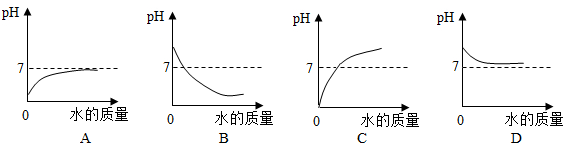
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水结成冰前后,质量保持不变 | |
| B. | 2g氢气在与8g氧气完全反应后可生成10g水 | |
| C. | 1.2g碳与3.2g氧气恰好完全反应可生成4.4g二氧化碳 | |
| D. | 在100g氢氧化钙溶液中,含有1g氢氧化钙和99g水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com