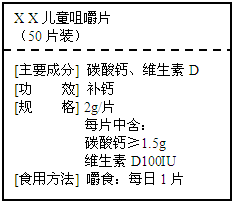
如图为“хх”钙片商品标签图,请根据标签的有关信息完成下列各题.

该钙片主要成分碳酸钙,主要成分碳酸钙由
种元素组成.碳酸钙中各元素的质量比为
.
每片钙片中至少含钙元素的质量为
.
某校化学兴趣小组为了确认标签中碳酸钙的含量是否真实,决定通过实验进行探究.
实验目标:测定该钙片主要成分碳酸钙的含量.
实验原理:取一定质量的钙片与足量的稀盐酸反应,测量生成的CO
2的质量(已知该状态下CO
2的密度),然后计算其中碳元素的质量,利用反应前后碳元素的质量不变,再计算出碳酸钙的质量.
实验方案:兴趣小组的同学们经过思考提出了以下几种实验方案,请你参与他们对实验方案的讨论、取舍.
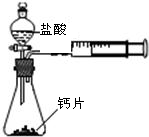
方案一;甲同学设计了如图所示的装置,通过反应后右侧注射器(注射器最大量程为20mL)内收集到气体
的量来进行计算.
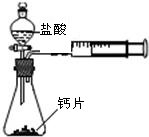
(1)同学们观看了他的设计后,都认为该方案中样品的取用的量需要一定的控制,这是因为
.
(2)同学们讨论后,一致认为注射器的摩擦会影响生成的CO
2的完全收集.
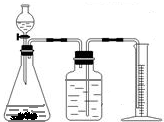
方案二:乙同学设计了如图所示的装置,与甲同学的相比,仅仅在收集方法上不同.
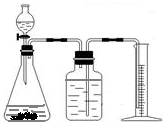
(1)同学们观看了他的设计后,都认为所测得CO
2气体的体积将会
(填偏大或偏小),你认为他们的理由是,会有部分二氧化碳溶解在水中,你的改进方案是
;广口瓶内原有的空气对实验结果
(填“有”或“没有”)影响
(2)同学们讨论后,一致认为把装置改进后测得生成的CO
2气体体积会偏大,你认为他们的最主要理由是
.
方案三:丙同学设计了如图所示的装置.同学们观看后一致认可他的设计,并按照他的思路设计了以下
实验步骤.
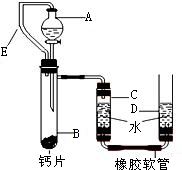
实验步骤:
①连接装置并检查装置气密性;
②加入10片钙片和水;
③记录C中液面刻度(C为带有刻度的玻璃管);
④由A向B中滴加稀盐酸至过量;
⑤待B中不再有气体产生并恢复至室温后,记录C中
液面刻度,计算得到气体的体积为V mL(经查,该气体密度为ρg/L);
⑥计算气体的质量.
实验反思:
(1)丙同学在实验前将钙片全磨成粉末状,你认为他的目的是:
;
(2)同学们都认为丙同学的设计中最经典的是连接仪器A和仪器B的橡胶管E,你认为橡胶管E的作用是:
;
(3)检查该装置的气密性时,如图准备好装置,在C、D两管中装好水且液面相平,提高D管,
,则气密性良好;
(4)通常实验前须估算药品用量,如果实验过程中,发现盐酸的量不足,应中途加酸还是重新实验:清判断并说明理由
.
实验结论:经多次实验(钙片都是10片),所得CO
2气体的平均质量是6.82g,请你最后计算确认标签中碳酸钙的含量是
(填“真实”或“不真实”)的.(最后一空不需要写计算过程)


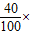 100%=0.496g.
100%=0.496g.





 如图是某钙片商品标签图.我能根据标签信息完成下列两题.
如图是某钙片商品标签图.我能根据标签信息完成下列两题. 如图是某钙片商品标签图.我能根据标签信息完成下列两题.
如图是某钙片商品标签图.我能根据标签信息完成下列两题.