

分析 结合给出的流程图和给予的信息提示进行问题的分析和解答,在解答中注意要紧扣生产流程的产品,过程中要减少杂质的引入.
解答 解:
(1)由于是处理废渣,使其中的锌完全转化,所以加入的酸应该是过量.在过程中通入空气根据给的“3FeO+10HNO3═3Fe(NO3)3+NO+5H2O,NO有毒,能与氧气和水反应生成硝酸”可知,一方面空气的鼓入会使固体在酸液中翻滚起到搅拌加大接触提高反应效率,另外一方面就是使有毒的NO和氧气接触进而转化成硝酸进一步去和废渣反应.对应的反应物为一氧化氮和氧气由于生成硝酸,根据质量守恒定律可知还有水作反应物,生成物只有硝酸,对应的化学方程式为:4NO+3O2+2H2O═4HNO3;
(2)由于最后要得到氧化锌,所以为了避免过程引入新的杂质,在给定的物质中氧化锌可以使用;
(3)废渣中含有ZnO、FeO、Fe2O3、CuO等杂质,而信息中“在“除杂Ⅰ”步骤中,只有铁离子能形成氢氧化铁沉淀”强调在除杂I中已经除掉了铁元素,所以只剩锌元素和铜元素,所以在除杂II中应该加入过量的锌让铜元素完全转化为单质而除去,所以得到的滤渣中含有生成的铜和剩余的锌.
(4)在“碳化合成”中,反应物为硝酸锌和碳酸钠和水(根据碱式碳酸锌中含有氢元素推测出来的),生成的产物之一为碱式碳酸锌[Zn2(OH)2CO3],还生成一种能使澄清石灰水变浑浊的气体氧化物(为二氧化碳),同时根据质量守恒定律可知还需要生成硝酸钠,对应的化学方程式为2Zn(NO3)2+2 Na2CO3+H2O═Zn2(OH)2CO3+4NaNO3+CO2↑.(配平时用先假设碱式碳酸锌的系数为1,配平其他)
故答案为:(1)使废渣完全反应;使NO转化为硝酸;4NO+3O2+2H2O═4HNO3;
(2)A;
(3)Zn Cu;
(4)2Zn(NO3)2+2 Na2CO3+H2O═Zn2(OH)2CO3+4NaNO3+CO2↑.
点评 给出的转化关系看起来很复杂,其实考查的问题是相对简单或者是熟悉的,所以解答时要从问题入手,也就是先看要解答的问题然后带着问题阅读题干,寻找解答的有效信息.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
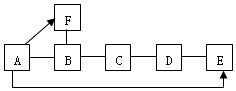 图中 B、C、D、E、F是初中化学常见的物质.A是铜绿的主要成分碱式碳酸铜【化学式为Cu2(OH)2CO3】,B是胃酸的主要成分,D、E、F都是氧化物,图中“-”表示两种物质能发生反应,“→”表示物质间的转化关系(部分反应物、生成物及反应条件已略去).若A在加热时可以生成F及D、E三种氧化物,B与C、C与D、B与F反应均可生成E.
图中 B、C、D、E、F是初中化学常见的物质.A是铜绿的主要成分碱式碳酸铜【化学式为Cu2(OH)2CO3】,B是胃酸的主要成分,D、E、F都是氧化物,图中“-”表示两种物质能发生反应,“→”表示物质间的转化关系(部分反应物、生成物及反应条件已略去).若A在加热时可以生成F及D、E三种氧化物,B与C、C与D、B与F反应均可生成E.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | O2 CO2 SO2 | B. | H2 O2 N2 | C. | CO2 SO2 HCl | D. | SO2 H2 N2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
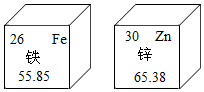 锌铁合金是一种具有特殊性能的材料,被广泛用于航天、航空、船舶、电子等工业部门,如图是锌、铁元素的部分信息,下列说法正确的是( )
锌铁合金是一种具有特殊性能的材料,被广泛用于航天、航空、船舶、电子等工业部门,如图是锌、铁元素的部分信息,下列说法正确的是( )| A. | 锌的金属活泼性比铁强的原因是锌原子的质子数比铁多 | |
| B. | 铁、锌元素的本质区别是电子数不同 | |
| C. | 锌原子的原子序数是30 | |
| D. | 铁的相对原子质量为55.85g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com