
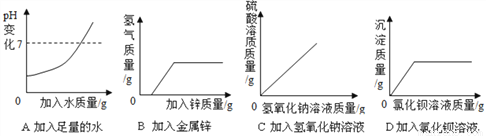
ĻņŅ»¶ØĮæµÄĮņĖįČÜŅŗÖŠ£¬·Ö±š¼ÓČė×ćĮæµÄĖ®”¢½šŹōŠæ”¢ĒāŃõ»ÆÄĘČÜŅŗ”¢ĀČ»Æ±µČÜŅŗ£¬ĻĀĮŠĶ¼Ź¾ÕżČ·µÄŹĒ ( )
A. A B. B C. C D. D
D ”¾½āĪö”æA”¢ĻņŅ»¶ØĮæµÄĮņĖįČÜŅŗÖŠ¼ÓČėĖ®£¬ĖįŠŌ¼õČõ£¬pHÖµ±ä“󣬵«pHÖµ²»ÄÜ“óÓŚ7£¬“ķĪó£»B”¢ĻņŅ»¶ØĮæµÄĮņĖįČÜŅŗÖŠ£¬¼ÓČė½šŹōŠæ£¬²śÉśĒāĘų£¬Ķ¼ĻńµÄĘšµćĪ»ÖĆÓ¦øĆ“ÓŌµćæŖŹ¼£¬“ķĪó£»C”¢ĻņŅ»¶ØĮæµÄĮņĖįČÜŅŗÖŠ£¬¼ÓČėĒāŃõ»ÆÄĘČÜŅŗ£¬ĮņĖįČÜÖŹÖŹĮæ¼õÉŁ£¬“ķĪó£»D”¢H2SO4 + BaCl2==BaSO4”ż+ 2HCl£¬³ĮµķÖŹĮæ“ÓĮćæŖŹ¼Öš½„Ōö¶ą£¬ĖłŅŌĶ¼ĻńµÄĘšµćĪ»ÖĆ“ÓŌµćæŖŹ¼£¬µ±Ļ”ĮņĖį·“Ó¦ĶźŅŌŗ󣬳ĮµķÖŹĮæ²»ŌŁŌö... ¼¤»īĖ¼Ī¬ÓżÓæĪĢĆĻµĮŠ“š°ø
¼¤»īĖ¼Ī¬ÓżÓæĪĢĆĻµĮŠ“š°ø »īĮ¦ŹŌ¾ķĻµĮŠ“š°ø
»īĮ¦ŹŌ¾ķĻµĮŠ“š°ø æĪæĪÓÅÄÜĮ¦ÅąÓÅ100·ÖĻµĮŠ“š°ø
æĪæĪÓÅÄÜĮ¦ÅąÓÅ100·ÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗÉĻŗ£ŹŠ³¤ÄžĒų2018½ģ¾ÅÄź¼¶ÖŠæ¼¶žÄ£»ÆѧŹŌ¾ķ ĢāŠĶ£ŗµ„Ń”Ģā
ÓŠ¹ŲĪ¢Į£µÄŠšŹöÕżČ·µÄŹĒ
A. øɱłÖŠµÄCO2 ·Ö×ÓŹĒ¾²Ö¹²»¶ÆµÄ
B. ±£³ÖĒāĘų»ÆѧŠŌÖŹµÄĪ¢Į£ŹĒĒā·Ö×Ó
C. ŃõĘų±ä³ÉŅŗŃõŹ±Ī¢Į£ÖŹĮæ±äŠ”ĮĖ
D. Ė®½į±łŗóĢå»ż±ä“óŹĒŅņĪŖĖ®·Ö×ÓĢå»żŌö“ó
B ”¾½āĪö”æA”¢øɱłÖŠµÄ CO2 ·Ö×Ó²»ŹĒ¾²Ö¹²»¶ÆµÄ£¬ŹĒÓĄ²»Ķ£Ļ¢µÄ×öĪŽ¹ęŌņŌĖ¶Æ£¬¹ŹA“ķĪó£»B”¢±£³ÖĒāĘų»ÆѧŠŌÖŹµÄĪ¢Į£ŹĒĒā·Ö×Ó£¬·Ö×ÓŹĒ±£³ÖĪļÖŹ»ÆѧŠŌÖŹµÄ×īŠ”Ī¢Į££¬¹ŹBÕżČ·£»C”¢ŃõĘų±ä³ÉŅŗŃõŹ±Ī¢Į£·Ö×Ó¼äøō±äŠ”ĮĖ£¬ÖŹĮæƻӊ±ä»Æ£¬¹ŹC“ķĪó£»D”¢Ė®½į±łŗóĢå»ż±ä“óŹĒŅņĪŖĖ®·Ö×Ó¼äøōŌö“󣬹ŹD“ķĪó”£ µć¾¦”Ć·Ö×ÓŹĒ±£³ÖĪļÖŹ»ÆѧŠŌÖŹµÄ×īŠ”Ī¢Į££¬ÓĄ²»Ķ£Ļ¢µÄ×öĪŽ¹ęŌņŌĖ¶Æ”£Īļ֏דĢ¬µÄ±ä»ÆŹĒ¹¹³ÉĪļÖŹĪ¢Į£¼äøō±ä»ÆµÄ...²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗÉĻŗ£ŹŠŠģ»ćĒų2018½ģ֊漶žÄ£»ÆѧŹŌ¾ķ ĢāŠĶ£ŗ¼ĘĖćĢā
²ŻÄ¾»ŅµÄÖ÷ŅŖ³É·ÖŹĒĢ¼Ėį¼Ų”£Ä³»ÆѧŠĖȤŠ”×éČ”100g²ŻÄ¾»ŅѳʷӌÉÕ±ÖŠ£¬²»¶ĻµĪČėĻ”ŃĪĖį£¬µ±ÉÕ±ÖŠµÄ²ŠÓą»ģŗĻĪļÖŹĮæĪŖ137.8gŹ±£¬³ä·Ö·“Ó¦”£·“Ó¦¹ż³Ģ·Å³öµÄĘųĢåÖŹĮæÓė¼ÓČėŃĪĖįµÄ¹ŲĻµĒśĻßČēĶ¼±ķŹ¾”£(¼ŁÉč²ŻÄ¾»ŅµÄĘäĖū³É·Ö²»ÓėĖį·“Ó¦)

Ēė¼ĘĖć»Ų“š£ŗ
(1)Ķ¼ÖŠ×Ż×ų±źÉĻaµćŹżÖµ£ŗa=__________g£»·Å³öĘųĢåµÄĪļÖŹµÄĮæĪŖ__________ mol”£
(2)²ŻÄ¾»Ņѳʷ֊Ģ¼Ėį¼ŲµÄÖŹĮæ·ÖŹżĪŖ________________(ŅŖĒ󊓳ö¼ĘĖć¹ż³Ģ)”£
2.2 0.05 6.9% ”¾½āĪö”æ(1)øł¾ŻÖŹĮæŹŲŗć¶ØĀÉ£¬a=100g+40g-137.8g=2.2g£¬Éś³ÉµÄĘųĢåŹĒ¶žŃõ»ÆĢ¼ĘųĢ壬¶žŃõ»ÆĢ¼µÄĪļÖŹµÄĮæĪŖ£ŗ=0.05mol (2)Éč²ŻÄ¾»Ņѳʷ֊Ģ¼Ėį¼ŲµÄÖŹĮæĪŖx”£ K2CO3 + 2HCl == 2KCl + H2O + CO2”ü 138 44 x 2.2g =£¬½āµĆx=6.9g ²ŻÄ¾»Ņѳʷ֊Ģ¼Ėį¼ŲµÄÖŹĮæ·ÖŹż...²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗÉĻŗ£ŹŠŠģ»ćĒų2018½ģ֊漶žÄ£»ÆѧŹŌ¾ķ ĢāŠĶ£ŗµ„Ń”Ģā
¹ę·¶µÄŹµŃé²Ł×÷ŹĒŹµŃé³É¹¦µÄ±ŲŅŖĢõ¼ž”£ĻĀĮŠŹµŃé²Ł×÷ÖŠ£¬ÕżČ·µÄŹĒ

A. A B. B C. C D. D
A ”¾½āĪö”æA”¢øųŹŌ¹ÜÖŠµÄŅŗĢå¼ÓČČ£¬ŹŌ¹ÜæŚŠ±ĻņÉĻ£¬ÓėĖ®Ę½·½Ļņ“óŌ¼³É45”£¼Š½Ē£¬ŅŗĢå²»Äܳ¬¹żŹŌ¹ÜČŻ»żµÄČż·ÖÖ®Ņ»£¬ŹŌ¹Ü¼Š¼ŠŌŚŹŌ¹ÜµÄÖŠÉĻ²æ£¬ÕżČ·£»B”¢µĪ¹ÜŌŚŹŌ¹ÜÉĻ·½ŠüæÕ“¹Ö±£¬“ķĪó£»C”¢ŹÓĻßÓė°¼ŅŗĆęµÄ×īµĶ“¦±£³ÖĖ®Ę½£¬“ķĪó£»D”¢ÓĆŪįŪöĒƼŠČ”Õō·¢Ć󣬓ķĪ󔣹ŹŃ”A”£²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ½ĖÕŹ”2018½ģ¾ÅÄź¼¶ĻĀѧʌŹŹÓ¦ŠŌÄ£Äā²āŹŌ»ÆѧŹŌ¾ķ ĢāŠĶ£ŗĮ÷³ĢĢā
CuCl2 ŹĒŅ»ÖÖ¹ć·ŗÓĆÓŚÉś²śŃÕĮĻ”¢Ä¾²Ä·ĄøƼĮµČµÄ»Æ¹¤²śĘ·”£¹¤ŅµÉĻŅŌ»ŌĶæó(Ö÷ŅŖŗ¬ÓŠ Cu2S”¢Fe2O3¼°Ņ»Š©²»ČÜŠŌŌÓÖŹ)ĪŖŌĮĻÖʱø CuCl2•2H2O ¾§ĢåµÄ¹¤ŅÕĮ÷³ĢČēĻĀ£ŗ
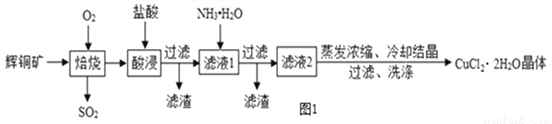
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)±ŗÉÕÖŠÉś³ÉŗŚÉ«¹ĢĢ壬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_______________________”£
(2)Ėį½žŹ±·¢ÉśµÄ»Æѧ·½³ĢŹ½ĪŖ___________________(Š“³öŅ»ÖÖ)£¬ĪŖ¼Óæģ·“Ó¦ĖŁĀŹ£¬ŅŌĻĀ“ėŹ©ĪŽ·Ø“ļµ½ÄæµÄŹĒ_________________”£
A£®ŃÓ³¤Ėį½žŹ±¼ä B£®½«»ŌĶæó·ŪĖé C£®ŹŹµ±Ōö¼ÓŃĪĖįÅضČ
(3)É«¹ā¶ČŹĒ²śĘ·ÖŹĮæÖø±źÖ®Ņ»£¬ŗĻøń CuCl2•2H2O ¾§ĢåµÄÉ«¹ā¶Č·¶Ī§ĪŖ-0.5”«0.5£¬·“Ó¦¹ż³ĢČÜŅŗ pH ¶Ō²śĀŹ”¢É«¹ā¶ČµÄÓ°Ļģ ČēĶ¼2ĖłŹ¾£¬×ŪŗĻæ¼ĀĒÖʱøŹ±Ó¦æŲÖĘ pH µÄ½ĻŗĻĄķ·¶Ī§ŹĒ____________”£
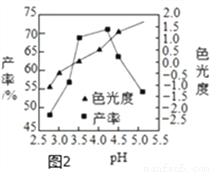
(4) CuCl2•2H2O ¾§ĢåæÉÓĆĀČ»ÆĶ±„ŗĶČÜŅŗĻ“µÓ¶ų²»ÓĆÕōĮóĖ®µÄŌŅņŹĒ_________”£
Cu2S+O22CuO+SO2 CuO + 2HCl ==CuCl2 + H2O£Ø»ņFe2O3 + 6HCl==2FeCl3 + 3H2O£© A 3.5-4.0 ·ĄÖ¹ĀČ»ÆĶČܽā£¬Ģįøß²śĀŹ ”¾½āĪö”æ(1)øßĪĀĢõ¼žĻĀ£¬Įņ»ÆŃĒĶŗĶŃõĘų·“Ӧɜ³ÉŃõ»ÆĶŗĶ¶žŃõ»ÆĮņ£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗCu2S+O22CuO+SO2 (2)Ėį½žŹ±£¬Ńõ»ÆĶŗĶĻ”ŃĪĖį·“Ӧɜ³ÉĀČ»ÆĶŗĶĖ®£¬Ńõ»ÆĢśÓėĻ”ŃĪĖį·“Ӧɜ³ÉĀČ»ÆĢśŗĶĖ®£¬·“Ó¦µÄ...²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ½ĖÕŹ”2018½ģ¾ÅÄź¼¶ĻĀѧʌŹŹÓ¦ŠŌÄ£Äā²āŹŌ»ÆѧŹŌ¾ķ ĢāŠĶ£ŗµ„Ń”Ģā
Čż¼×»łŅ»ĀČ¹č[(CH3)3SiCl]ŹĒŅ»ÖÖÉś²śÓŠ»ś¹č»ÆŗĻĪļµÄŌĮĻ£¬Óö»šÄÜČ¼ÉÕÉõÖĮ»į·¢Éś±¬ÕØ£¬ÓėĖ®½Ó“„æɲśÉśŃĪĖį”£ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ ( )
A. ±£“ęČż¼×»łŅ»ĀČ¹čŹ±Ó¦ĆÜ·ā·ĄĖ®
B. Čż¼×»łŅ»ĀČ¹čÖŠĢ¼”¢ĒāŌŖĖŲÖŹĮæ±ČĪŖ4£ŗ1
C. Čż¼×»łŅ»ĀČ¹čÓÉ4ÖÖŌŖĖŲ×é³É
D. Čż¼×»łŅ»ĀČ¹čÓÉĢ¼”¢Ēā”¢¹č”¢ĀČ¹²14øöŌ×Ó¹¹³É
D ”¾½āĪö”æA. Čż¼×»łŅ»ĀČ¹čÓėĖ®½Ó“„æɲśÉśŃĪĖį£¬ĖłŅŌ±£“ęČż¼×»łŅ»ĀČ¹čŹ±Ó¦ĆÜ·ā·ĄĖ®£¬ÕżČ·£»B. Čż¼×»łŅ»ĀČ¹čÖŠĢ¼”¢ĒāŌŖĖŲÖŹĮæ±ČĪŖ12£ŗ£Ø1”Į3£©=4:1£¬ÕżČ·£»C. Čż¼×»łŅ»ĀČ¹čÓÉC”¢H”¢Si”¢ClĖÄÖÖŌŖĖŲ×é³É£¬ÕżČ·£»D. Ņ»øöČż¼×»łŅ»ĀČ¹č·Ö×ÓÓÉ3øöĢ¼Ō×Ó”¢9øöĒāŌ×Ó”¢1øö¹čŌ×Ó”¢1øöĀČŌ×Ó¹²14øöŌ×Ó¹¹³É£¬“ķĪ󔣹ŹŃ”D”£²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗŗŚĮś½Ź”“óĒģŹŠ¶Å¶ū²®ĢŲĻŲ2018½ģ¾ÅÄź¼¶£Ø³õĖÄ£©ĻĀŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ ĢāŠĶ£ŗ¼ĘĖćĢā
ŌŚĮņĖįÓėĮņĖįĶµÄ»ģŗĻČÜŅŗ200gÖŠ£¬µĪČė40%µÄNaOHČÜŅŗ100g£¬Ē”ŗĆĶźČ«·“Ó¦£¬¼ĒĀ¼·“Ó¦¹ż³Ģ£¬µĆµ½µÄ³ĮµķÓėĖł¼ÓµÄĒāŃõ»ÆÄĘČÜŅŗµÄÖŹĮæ¹ŲĻµČēĶ¼ĖłŹ¾£®

»Ų“š£ŗ
(1)ÓėĮņĖįĶ·“Ó¦µÄĒāŃõ»ÆÄĘČÜŅŗµÄÖŹĮæĪŖ__________g”£
(2)“ĖĮņĖįµÄČÜÖŹÖŹĮæ·ÖŹżĪŖ________£æ
(3)·“Ó¦ŗóČÜŅŗČÜÖŹµÄÖŹĮæ·ÖŹżŹĒ_________________”£
50g 12.25% 25.8% ”¾½āĪö”æ£Ø1£©øł¾ŻĶ¼ĻóæÉŅŌ擳ö£¬µ±ĒāŃõ»ÆÄĘČÜŅŗµÄÖŹĮæĪŖ50æĖŹ±£¬³ĮµķæŖŹ¼³öĻÖ£»µ±ĒāŃõ»ÆÄĘČÜŅŗµÄÖŹĮæĪŖ100æĖŹ±£¬³ĮµķµÄÖŹĮæ“ļµ½×ī“óÖµ”£ĖłŅŌÓėĮņĖįĶ·“Ó¦µÄĒāŃõ»ÆÄĘČÜŅŗµÄÖŹĮæĪŖ£Ø100-50£©æĖ£¬(1)ÓɵƵ½µÄ³ĮµķÓėĖł¼ÓµÄĒāŃõ»ÆÄĘČÜŅŗµÄÖŹĮæ¹ŲĻµĶ¼£¬æɲéµĆÓė»ģŗĻČÜŅŗÖŠĮņĖį·¢Éś·“Ó¦µÄĒāŃõ»ÆÄĘČÜŅŗÖŹĮæĪŖ50g£» (2)ÉčĻūŗÄĮņĖįµÄÖŹĮæĪŖx£¬Éś³ÉĮņĖįÄʵÄÖŹĮæĪŖy ...²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗŗŚĮś½Ź”“óĒģŹŠ¶Å¶ū²®ĢŲĻŲ2018½ģ¾ÅÄź¼¶£Ø³õĖÄ£©ĻĀŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ ĢāŠĶ£ŗµ„Ń”Ģā
Š”Ć÷Ķ¬Ń§ŌŚ¼ŅĄļÉč¼ĘĮĖŅŌĻĀ”°¼ŅĶ„Š”ŹµŃé”±·½°ø£¬ĘäÖŠ²»æÉŠŠµÄŹĒ( )
A. ÓĆĶĖæµČ²ÄĮĻĢ½¾æĶÉśŠāµÄĢõ¼ž
B. ÓĆ·ŹŌķĖ®¼ų±š¼ŅĶ„ÓĆĖ®ŹĒ·ńŹĒÓ²Ė®
C. ÓĆÉÕ¼īČÜŅŗ½žÅŻŹ÷Ņ¶ÖĘ×÷”°Ņ¶ĀöŹéĒ©”±
D. ÓĆ×ŌÖĘ¾»Ė®Ę÷°Ń»ė×ĒµÄŗÓĖ®±ä³É“æ¾»Ė®
D ”¾½āĪö”æA”¢ĶÉśŠāµÄĢõ¼žŹĒĖ®”¢ŃõĘųŗĶ¶žŃõ»ÆĢ¼µÄ¹²Ķ¬×÷ÓĆ£¬ĖłŅŌæÉŌŚ¼Ņ½ųŠŠ£¬ÕżČ·£»B”¢Ó²Ė®ÖŠ¼ÓČė·ŹŌķ£¬²śÉśµÄÅŻÄŗÜÉŁ£¬»¹»įŠĪ³É°×É«¹øדĪļ£»¶ųČķĖ®¼ÓČė·ŹŌķ£¬²śÉśµÄÅŻÄ¶ą£¬¹ŹæÉĒų·Ö£¬ÕżČ·£»C”¢Ź÷Ņ¶µÄŅ¶ĀöÖŠŗ¬ÓŠÖ²ĪļĖį»ņ¼ī£¬æÉŅŌŗĶĒāŃõ»ÆÄĘ·¢ÉśĻŌÉ«·“Ó¦£¬ÕżČ·£»D”¢×ŌÖĘ¾»Ė®Ę÷ÄܳżČ„Ė®ÖŠµÄ²»ČÜŠŌŌÓÖŹ£¬³ż²»Č„æÉČÜŠŌŌÓÖŹ£¬µĆ²»µ½“æĖ®£¬“ķĪ󔣹ŹŃ”D”£²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ½ĖÕŹ”³£ŹģŹŠ2018½ģ¾ÅÄź¼¶ĻĀѧʌŹŹÓ¦ŠŌÖŹĮæ¼ģ²ā»ÆѧŹŌ¾ķ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠĪļÖŹµÄ¼ų±š·½·Ø“ķĪóµÄŹĒ
Ń”Ļī | “ż¼ų±šµÄĪļÖŹ | ¼ų±š·½·Ø |
A | ÄįĮśŗĶŃņĆ« | Ȕѳ£¬µćČ¼ |
B | ĮņĖįĶŗĶĮņĖįÄĘ | Ȕѳ£¬¼ÓĖ® |
C | ¹żŃõ»ÆĒāČÜŅŗŗĶĖ® | Ȕѳ£¬¼Ó¶žŃõ»ÆĆĢ |
D | ĀČ»Æļ§ŗĶĻõĖįļ§ | Ȕѳ£¬¼ÓŹģŹÆ»Ņ£¬ŃŠÄ„ |
A. A B. B C. C D. D
D ”¾½āĪö”æA”¢Č”ѳʷ£¬Č¼ÉÕ£¬»į²śÉśÉÕ½¹ÓšĆ«ĘųĪ¶µÄĘųĢåµÄŹĒŃņĆ«£¬Ć»ÓŠ“ĖĘųĪ¶µÄŹĒÄįĮś£¬ĻÖĻó²»Ķ¬£¬æÉŅŌ¼ų±š£¬ÕżČ·£»B”¢Č”ѳʷ£¬¼ÓĖ®Čܽā£¬ČÜŅŗĻŌĄ¶É«µÄŹĒĮņĖįĶ£¬ČÜŅŗĪŽÉ«µÄŹĒĮņĖįÄĘ£¬ĻÖĻó²»Ķ¬£¬æÉŅŌ¼ų±š£¬ÕżČ·£»C”¢Č”ѳʷ£¬¼ÓČė¶žŃõ»ÆĆĢ£¬ÓŠĘųĢå²śÉśµÄŹĒ¶žŃõ»ÆĆĢ£¬ĪŽĘųĢå²śÉśµÄŹĒĖ®£¬ĻÖĻó²»Ķ¬£¬æÉŅŌ¼ų±š£¬ÕżČ·£»D”¢Č”ѳʷ£¬¼ÓČėŹģŹÆ»ŅŃŠÄ„£¬¶¼»įÉś³É°±Ęų£¬ĻÖĻóĻąĶ¬£¬²»Äܼų±š£¬“ķĪ󔣹ŹŃ”D”£²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com