
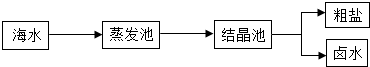

分析 (1)根据在蒸发池中,水蒸发了,溶剂的质量减少,溶质的质量不变进行分析;
(2)根据①处发生的反应是氯化镁和氢氧化钙反应生成氢氧化镁沉淀和氯化钙进行分析;
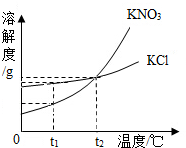
(3)根据氯化钾和硝酸钾的溶解度曲线进行分析;
运用溶解度曲线上的交点是该温度下物质的溶解度相等解答;
根据物质的溶解度受温度的影响情况来分析;
根据20℃时,KNO3的溶解度为31.6g;80℃时,KNO3的溶解度为169g进行分析.
解答 解:(1)在蒸发池中,水蒸发了,溶剂的质量减少,溶质的质量不变;故填:不变;
(2)①处发生的反应是氯化镁和氢氧化钙反应生成氢氧化镁沉淀和氯化钙,属于复分解反应;故填:复分解;
(3)①通过分析溶解度曲线,可以看出,t1℃时,氯化钾的溶解度大于硝酸钾的溶解度,所以KCl饱和溶液的溶质质量分数大于KNO3饱和溶液的溶质质量分数;
故填:大于;
②t2℃时,氯化钾和硝酸钾两物质的溶解度曲线相交,说明该温度下二者的溶解度相等,故答案:t2℃时,氯化钾和硝酸钾两物质的溶解度相等;
③KNO3的溶解度受度变化影响较大,KCl的溶解度受温度影响较小,所以若KNO3中混有少量KCl,可利用降温结晶的方法提纯KNO3;故填:降温结晶;
④20℃时,KNO3的溶解度为31.6g;80℃时,KNO3的溶解度为169g,在20℃时,向盛有200g水的烧杯中加入80gKNO3,溶解的硝酸钾为63.2g,所以得到该温度时KNO3的饱和溶液,若使烧杯内物质缓慢升温至80℃,在该温度下,固体全部溶解,所以最后所得溶液中溶质与溶剂的质量之比为80g:200g=2:5.
故填:饱和;2:5.
点评 本题考查了据溶解度曲线的意义和饱和溶液中溶质的质量分数分析解答问题,难度不大.


 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:初中化学 来源: 题型:选择题
| A. | H、D、T相对原子质量之比为1:2:3 | |
| B. | LiH、LiD、LiT相对分子质量相同 | |
| C. | H、D、T化学性质不同 | |
| D. | LiH、LiD、LiT中Li元素质量分数相等 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 某同学研究温度和pH对某酶反应催化作用速率的影响,得到如图的曲线.下列分析正确的是( )
某同学研究温度和pH对某酶反应催化作用速率的影响,得到如图的曲线.下列分析正确的是( )| A. | 该酶催化反应的最适温度为35℃左右,最适pH为8 | |
| B. | 当pH为8时,影响反应速率的主要因素是底物浓度和酶浓度 | |
| C. | 随pH升高,该酶催化反应的最适温度也逐渐升高 | |
| D. | 当pH为任何一固定值时,实验结果都可以证明温度对反应速率的影响 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
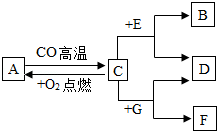 现有A、B、C、D、E、F、G七种物质,C、F是最常见的金属,B是气体单质,D为浅绿色溶液,G为蓝色溶液,它们之间存在如图关系:
现有A、B、C、D、E、F、G七种物质,C、F是最常见的金属,B是气体单质,D为浅绿色溶液,G为蓝色溶液,它们之间存在如图关系:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com