
碳酸钠和碳酸氢钠的固体混合物充分加热至恒重,其质量变化如下图所示。另取相同质量的该混合物溶于水得到106.6 g溶液,向该溶液中加入100 g 7.3% 的稀盐酸,恰好完全反应。(已知:2NaHCO3 Na2CO3+CO2↑+H2O,碳酸钠受热不易分解。)
计算:(1)混合物与盐酸反应生成二氧化碳的质量。
(2)所得溶液中溶质的质量分数。

【解析】由图可知固体减少的质量是生产二氧化碳和水的质量,然后根据质量守恒定律进行解答。
【答案】解:设混合物中碳酸氢钠的质量为x ; 碳酸氢钠与盐酸反应生成二氧化碳的质量为y、碳酸钠与盐酸反应生成二氧化碳的质量为z
碳酸氢钠与盐酸反应生成二氧化碳的质量为y、碳酸钠与盐酸反应生成二氧化碳的质量为z
2NaHCO3 Na2CO3+CO2↑+H2O
2×84 (44 + 18)
x 3.1 g
|
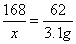
x = 8.4g
NaHCO3 +HCl = NaCl + CO2↑+H2O
84 44
8.4 g y
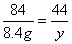
y = 4.4g
混合物中碳酸钠的质量为:13.7g -8.4g = 5.3g
Na2CO3 +2HCl = 2NaCl + CO2↑+H2O
106 44
5.3 g z
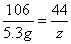
z = 2.2g
13.7 g混合物与稀盐酸反应生成二氧化碳的总质量是6.6 g
反应后溶液的质量:106.6 g+100 g-6.6 g = 200 g,
根据氯元素守恒,设反应生成氯化钠的质量为m
HCl ~ NaCl
36.5 58.5
100 g× 7.3% m
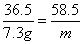
m = 11.7g
氯化钠溶液中氯化钠的质量分数= 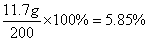
答:混合物与盐酸反应生成二氧化碳的质量为6.6g;与盐酸反应后溶液中氯化钠的质量分数是5.85%。


 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:初中化学 来源: 题型:阅读理解
| ||
| ||
| 加热 |
| 加热 |
查看答案和解析>>
科目:初中化学 来源:江苏省兴化市2011届九年级网上阅卷适应性训练化学试题 题型:058
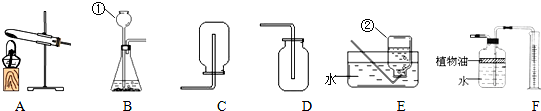
下列为实验室常用的实验装置,回答问题:
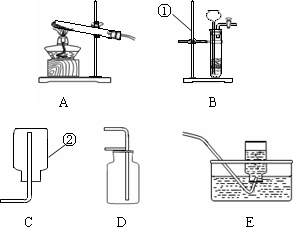
(1)写出带有标号仪器的名称:①________;②________.
(2)用锌和稀硫酸制取氢气,应选用的发生装置是
________(填序号,下同),收集装置是________.(3)实验室常用稀盐酸和石灰石反应制CO2,该反应的化学方程式________;
此外,也可用加热碳酸氢钠(NaHCO3)固体(产物为碳酸钠、二氧化碳、水)来制取CO2,该反应的化学方程式________,若用此法来制取CO2,应选用的发生装置为________,收集装置为________.
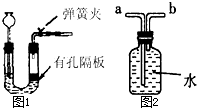
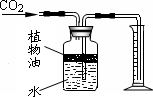
(4)下图所示装置可用来测量生成的CO2的体积,其中在水面上放一层植物油的目的是________,植物油上方原有的空气对实验结果________(填“有”或“无”)明显影响.
(5)化学上可通过多种反应得到NH3(极易溶于水,密度比空气小),例如:
a.2NH4Cl(
固)+Ca(OH)2(固)b.NH4HCO3(
固)c.CaO(
固)+NH3·H2O=NH3↑+Ca(OH)2结合以上实验装置完成下列填空(以下均填序号):
我将选择上述反应________作为实验室制取NH3的反应原理,选用上图中的________作为反应的发生装置,采用的收集装置是________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com