
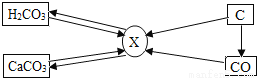
碳和碳的化合物间的部分转化关系如图所示.则下列说法正确的是( )
A. 由碳酸转化成X一定要在加热条件下进行
B. 由碳转化为X一定发生的是化合反应
C. 物质X一定是二氧化碳
D. 若使一氧化碳转化成X,只能通过一氧化碳在空气(或氧气)中燃烧获得
C 【解析】由转化关系图可知,碳酸分解生成二氧化碳,二氧化碳与水反应生成碳酸,故X是二氧化碳。A、碳酸在常温下就容易分解生成二氧化碳,错误;B、在高温的条件下,碳能与氧化铜反应生成铜和二氧化碳,该反应属置换反应,错误;C、X是二氧化碳,正确;一氧化碳转化为二氧化碳的方法有:燃烧法、一氧化碳还原氧化铁或还原氧化铜,错误。故选C。科目:初中化学 来源:四川省眉山市2018届九年级中考模拟(一)化学试卷 题型:单选题
下列有关溶液的说法正确的是
A.降低饱和溶液的温度,一定有晶体析出
B.长期放置后不会分层的液体一定是溶液
C.KNO3饱和溶液一定比不饱和溶液溶质质量分数大
D.配制好6%的NaCl溶液,装瓶时不小心洒漏一部分,瓶中NaCl溶液浓度仍为6%
D 【解析】A、降低饱和溶液的温度,不一定有晶体析出,比如氢氧化钙的饱和溶液升高温度溶解度升高,没有晶体析出,错误; B、长期放置后不会分层的液体不一定是溶液,比如水,错误; C、在同一温度下,KNO3饱和溶液一定比不饱和溶液溶质质量分数大,错误; D、溶液具有均一性,故将配制好6%的NaCl溶液,装瓶时不小心洒漏一部分,瓶中NaCl溶液浓度仍为6%,正确; 故选D....查看答案和解析>>
科目:初中化学 来源:山东省临沂市蒙阴县2018届九年级二轮验收化学试卷 题型:简答题
下图中,①是钠元素在元素周期表中的信息,A、B、C是三种粒子的结构示意图。试回答下列问题:
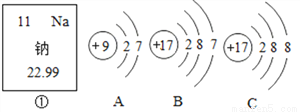
(1)钠元素的原子序数为______;
(2)A、B、C中属于同种元素的粒子是_________(填字母编号);
(3)A和B两种粒子的_________________相同,所以它们有相似的化学性质;
(4)C所表示的粒子是_______________(填“原子”或“离子”)。
11 BC 最外层电子数 离子 【解析】本题考查了元素周期表的特点及其应用,原子结构示意图与离子结构示意图。在原子中,原子序数,质子数,核外电子数,核电荷数之间的关系及元素的最外层电子数决定元素的化学性质的理解与掌握是解题的基础。 (1)由钠元素的元素周期表中的信息可知钠元素的原子序数为11; (2)根据决定元素种类的是核电荷数(即核内质子数),因为BC的核内质子数相同,所以BC...查看答案和解析>>
科目:初中化学 来源:山东省临沂市蒙阴县2018届九年级二轮验收化学试卷 题型:单选题
空气是一种宝贵的资源,下列有关空气的说法正确的是
A.氮气化学性质不活泼,可用于食品防腐
B.稀有气体常用于医疗急救
C.二氧化碳在空气中含量增多会引起温室效应,属于空气污染物
D.氧气的化学性质比较活泼,属于可燃物
A 【解析】A.氮气化学性质不活泼,可用于填充食品包装袋内,隔绝氧气防止食物因缓慢氧化而变质;B.氧气能常用于医疗急救;C.二氧化碳在空气中含量增多会引起温室效应,但不属于空气污染物;D.氧气的化学性质比较活泼,属于助燃物;选A查看答案和解析>>
科目:初中化学 来源:广东省深圳市宝安区2018届年九年级一模化学试卷 题型:推断题
如图所示A是氧化物,可作干燥剂;已知F、K常温下为无色液体,且组成元素相同,G、L、X、E都为黑色固体,X、E为单质,G、L为氧化物。(通常情况下)B、D、H为气体,它们之间发生如图变化,请你根据所学的化学知识作出推断:
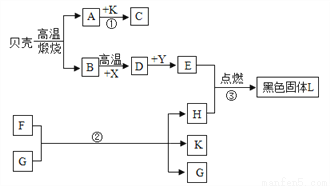
(1)反应①由A→C的过程是__________(“放出”或“吸收”)热量的;
(2)贝壳的主要成分是___________(写名称),贝壳高温煅烧的化学方程式___________;
(3)B→D的化学方程式___________________;
(4)B的固态的用途是______________;
(5)E与H生成L的现象是______________________________。
放出 碳酸钙 CaCO3CaO+CO2↑ CO2+C 2CO 人工降雨(合理即可) 剧烈燃烧,放出大量的热,火星四射,生成黑色固体 【解析】本题属于推断题,根据题目给出的流程图和信息:贝壳的主要成分是碳酸钙,碳酸钙在高温下生成氧化钙和二氧化碳,A是氧化物,可作干燥剂, A是氧化钙,B是二氧化碳;氧化钙和水生成氢氧化钙,已知F、K常温下为无色液体,且组成元素相同,则C是氢氧化钙,F是过氧化氢,...查看答案和解析>>
科目:初中化学 来源:广东省深圳市宝安区2018届年九年级一模化学试卷 题型:单选题
关于物质的溶解性及溶解度,下列说法正确的是( )
A. 喝了汽水常常会打嗝,这说明温度升高,气体的溶解度增大
B. 所有物质的溶解度只受温度影响
C. 0℃时,硝酸钾的溶解度是13.3g,所以硝酸钾属于可溶物质
D. 同种物质在不同溶剂中的溶解性是不同的,例如碘在水中溶解性小,而在汽油中溶解性大
D 【解析】A、喝了汽水,常常打嗝,这说明温度升高,气体的溶解度减小,错误;B、影响物质溶解度因素有溶质、溶剂性质和温度,错误;C、判定物质是否是可溶的依据是物质在20℃时的溶解度,不是0℃时的溶解度,错误;D、同种物质在不同溶剂中的溶解性是不同的,例如碘在水中溶解度小,而在汽油中溶解度大,正确。故选D。查看答案和解析>>
科目:初中化学 来源:广东省深圳市宝安区2018届年九年级一模化学试卷 题型:单选题
下列关于空气的说法中,正确的是( )
A. 空气的成分按质量分数从大到小为:N2 78%、O2 21%、稀有气体0.94%、CO2 0.03%
B. 液化空气中分离出的氮气化学性质不活泼,食品包装袋中充氮气可以防腐
C. 硫在空气中燃烧的现象是:发出淡蓝色的光,生成刺激性气味的二氧化硫
D. 二氧化碳是温室气体,属于大气污染物
B 【解析】A、空气中各成分的体积分数分别是:氮气大约占78%、氧气大约占21%、稀有气体0.94%、CO20.03%,不是按质量计算,错误;B、氮气的化学性质不活泼,无毒,食品包装中可充氮气防腐,正确;C、硫在空气中燃烧生成刺激性气味的二氧化硫属于实验结论,不是实验现象,错误;D、二氧化碳是空气的一种成分,不是大气污染物,错误。故选B。查看答案和解析>>
科目:初中化学 来源:四川省成都高新区2018年中考化学模拟测试卷 题型:填空题
(6分)下表是Ca(OH)2和NaOH的溶解度数据。请回答下列问题:
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
NaOH | 31 | 91 | 111 | 129 | 313 | 336 |
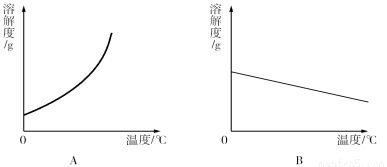
(1)依据上表数据,绘制了Ca(OH)2和NaOH的溶解度曲线,下图中能表示NaOH溶度曲线的是 (填“A”或“B”);
(2)将一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:
①加入氢氧化钙 ②升高温度 ③降低温度 ④加入水 ⑤蒸发水后再恢复到原温度 ⑥加入生石灰。
其中措施正确的是 ;
A.②④⑥ B.③④ C.①③⑤⑥ D.①②⑤⑥
(3)20℃时,191g饱和NaOH溶液,蒸发10g水后,再恢复到20℃,可析出NaOH固体的质量为 ;
(4)现有20℃时Ca(OH)2的饱和溶液甲,向其中加入一定量CaO后得到溶液乙,此时溶液中溶质的质量
乙 甲(填“>”、“<”或“=”);
(5)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH固体,应采取的物理方法是 ;
(6)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH (填“偏大”、“偏小”或“不受影响”)。
(1) A (2) D (3) 9.1g (4)< (5)降温结晶,过滤 (6)偏小 【解析】 试题分析:(1)由表格数据可知,氢氧化钠的溶解度随温度的升高而增大,氢氧化钙的溶解度随温度的升高而减小,故A表示的是氢氧化钠的溶解度曲线,B表示的是氢氧化钙的溶解度曲线; (2)将一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,方法有:加入溶质氢氧化钙或恒温蒸发溶剂水或升高温度,由于氧化...查看答案和解析>>
科目:初中化学 来源:江苏省泰兴市2018届九年级二模化学试卷 题型:科学探究题
甲、乙两同学对镁与盐酸反应进行系列研究。
甲、乙两同学取一根镁条,首先用砂纸打磨除去_______,观察到镁条的颜色_______。
研究Ⅰ:镁与盐酸反应过程中的能量变化以及反应速率的变化。
(1)反应中试管外壁发烫,说明镁与稀盐酸反应是_______反应(填“吸热”或“放热”),反应的化学方程式是________。
(2)实验测得镁片产生气体的速率(v)与时间(t)的关系如图所示,
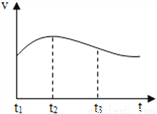
则t1-t2内反应速率逐渐加快的主要原因是________;
反思:t2-t3内反应速率逐渐减慢的主要原因是_________;
研究Ⅱ:反应后所得溶液的酸碱性探究。
(3)用pH试纸测定反应后所得溶液的酸碱度,发现pH略小于7。
甲同学:猜想Ⅰ:稀盐酸过量;猜想Ⅱ:氯化镁溶液呈弱酸性。
用pH试纸测定酸酸碱度的方法是_______。为验证猜想Ⅱ正确,可以通过查阅资料,也可以取纯净的________溶液并测定其酸碱度。
(4)乙同学将镁片(有剩余)投入适量稀盐酸,待不再产生气泡时立即测量pH,却发现所得溶液pH大于7,溶液冷却到室温后pH小于7。查阅资料发现①Mg+2H2O=Mg(OH)2↓+H2↑,②20℃时SMg(OH)2=0.009g,80℃时 SMg(OH)2=0.0108g。根据资料,乙同学实验中pH发生变化的原因是__________。
表面的氧化膜(或氧化膜) 银白色 放热 Mg+2HCl=MgCl2+H2↑ 温度升高,反应速度加快 浓度降低,反应速度减慢 将待测液滴在pH试纸上,并与标准比色卡对比,读出读数 MgCl2 温度较高时Mg(OH)2溶解度大,溶液因Mg(OH)2而显碱性,室温时Mg(OH)2溶解度太小,溶液因MgCl2而显酸性 【解析】镁是活泼金属,故易于空气中的氧气反应,表面生成了氧化膜,故在实验中要先用砂...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com