
| 实验步骤 | 实验现象 | 实验结论 |
| 样品为铵态氮肥 |
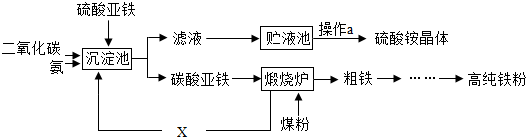
分析 (1)根据一氧化碳具有还原性,能将金属氧化物还原为金属单质来分析;
(2)根据实验流程图可知,X是二氧化碳;
(3)根据铵根离子的检验方法来分析.
解答 解:(1)一氧化碳具有还原性,在高温的条件下能将氧化亚铁还原为铁和二氧化碳;故填:将铁从氧化亚铁中还原出来;FeO+CO$\frac{\underline{\;高温\;}}{\;}$ Fe+CO2
(2)X是碳酸亚铁分解生成的二氧化碳,二氧化碳重新利用,可以减少温室气体的排放,降低温室效应;故填:减少温室气体CO2的排放(或降低生产成本)(合理均对);
(3)由于铵盐遇碱会生成氨气,所以可设计硫酸铵与消石灰共同研磨,从产生刺激性气味分析设计;
故答案为:
| 实验步骤 | 实验现象 | 实验结论 |
| 取适量样品,放在研钵中,加入 少量消石灰,混合研磨,用湿润的红色石蕊试纸检测产生的气体 | 产生刺激性的氨臭味气体,试纸变蓝 | 样品为铵态氮肥 |
点评 本题考查了物质的制备,解答时,根据流程图结合反应的原理来分析解答.


科目:初中化学 来源: 题型:选择题
| A. | 赤铜矿(Cu2O) | B. | 辉铜矿(Cu2S) | C. | 斑铜矿(Cu3FeS4) | D. | 孔雀石[Cu2(OH)2CO3] |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
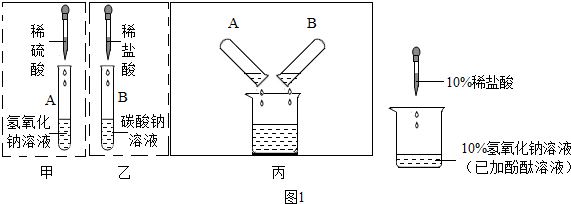
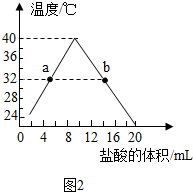
| 实验过程 | 实验现象 | 实验结论 |
| 向盛有少量Fe2CO3的试管中分别加入NaCl溶液和Na2SO4溶液,振荡 | 固体不溶解 | ${SO}_{4}^{2-}$或Cl-不能使Fe2O3溶解;H2O分子不能使Fe2O3溶解 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 锌 | B. | 钛 | C. | 镁 | D. | 锰 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com