(2010?天津)将铁粉和铜粉的混合物7g,加入到盛有58.1g稀盐酸的烧杯中,恰好完全反应.此时烧杯内各物质的总质量为64.9g.试计算:
(1)原混合物中铁粉的质量分数;
(2)反应后所得溶液中溶质的质量分数;
(3)配制上述反应中所用稀盐酸需要质量分数为38%的浓盐酸(密度为1.19g/cm3)的体积.(计算结果精确到0.1)
【答案】
分析:(1)混合物中铁粉与稀盐酸反应放出氢气而使反应前后烧杯内各物质的总质量减小,根据质量守恒定律,反应前后烧杯内各物质的总质量差即放出氢气的质量;由生成氢气的质量,根据反应的化学方程式,计算参加反应铁的质量,再由铁的质量与混合物的质量比计算混合物中铁粉的质量分数;
(2)由生成氢气的质量,根据反应的化学方程式,计算恰好反应时生成氯化亚铁的质量,再由氯化亚铁的质量与反应所得溶液的质量比计算反应后所得溶液中溶质的质量分数;反应后溶液的质量=完全反应后烧杯内各物质的总质量为64.9g-未参加反应的铜的质量;
(3)根据加水稀释前后溶液中溶质质量不变,由反应计算恰好完全反应时消耗HCl的质量,由消耗HCl的质量与所用浓盐酸的质量分数为38%计算需要浓盐酸的质量,并利用m=ρV计算浓盐酸的体积.
解答:解:根据质量守恒定律,生成氢气的质量=7g+58.1g-64.9g=0.2g;
设混合物中铁的质量为x,生成氯化亚铁的质量为y,参加反应的HCl的质量为z
Fe+2HCl═FeCl
2+H
2↑
56 73 127 2
x z y 0.2g

=
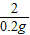
x=5.6g
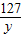
=
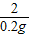
y=12.7g
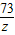
=
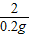
z=7.3g
原混合物中铁粉的质量分数=
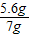
×100%=80%
反应后所得溶液中溶质的质量分数=
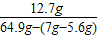
×100%=20%
需要质量分数为38%的浓盐酸(密度为1.19g/cm
3)的体积=
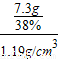
=16.1mL
答:(1)原混合物中铁粉的质量分数为80%;
(2)反应后所得溶液中溶质的质量分数为20%;
(3)需要质量分数为38%的浓盐酸的体积为16.1mL.
点评:根据化学方程式能表示反应中各物质的质量关系,由反应中其中任意物质的质量可以计算反应中其它物质的质量.

 =
=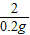 x=5.6g
x=5.6g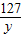 =
=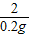 y=12.7g
y=12.7g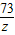 =
=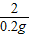 z=7.3g
z=7.3g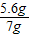 ×100%=80%
×100%=80%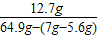 ×100%=20%
×100%=20%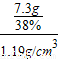 =16.1mL
=16.1mL

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案