
分析 本题涉及两个化学反应方程式:Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 和 CO2+Ca(OH)2═CaCO3↓+H2O,二者之间可通过二氧化碳相联系,根据后一个方程式15g白色沉淀,即生成15g碳酸钙的质量可以求出二氧化碳的质量,再根据二氧化碳的质量,利用前一个方程式可求出氧化铁的质量,进一步可求出样品中Fe2O3的质量分数.
解答 解:CO还原Fe2O3生成铁和二氧化碳,化学方程式为:Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 ;
设生成4.0g碳酸钙需要二氧化碳的质量为w
CO2+Ca(OH)2═CaCO3↓+H2O
44 100
x 4.0g
$\frac{44}{w}=\frac{100}{4.0g}$
w=1.76g
设生成1.76g二氧化碳需要Fe2O3的质量为x
Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
160 132
x 1.76g
$\frac{160}{x}=\frac{132}{1.76g}$
y=2.13g
赤铁矿样品中Fe2O3的质量分数为:$\frac{2.13g}{3.0g}$×100%=71%
答:赤铁矿样品中Fe2O3的质量分数为71%.
故答案为:(1)Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 ;
(2)$\frac{160}{x}=\frac{132}{1.76g}$
(3)71%
点评 本题考查有关化学反应方程式的计算,在计算时一定要找准相关量之间的对应关系.


 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案科目:初中化学 来源: 题型:解答题
 已知:反应①是实验室制取气体A的常用方法,D常用来改良酸性土壤,它们之间的转化关系如图所示(部分物质和反应条件已略去).图示关系中未涉及到的基本反应类型为置换反应;化学方程式①为CaCO3+2HCl═CaCl2+H2O+CO2↑; ②为CaO+H2O═Ca(OH)2;B在生产或生活中的一种用途是用作建筑材料.
已知:反应①是实验室制取气体A的常用方法,D常用来改良酸性土壤,它们之间的转化关系如图所示(部分物质和反应条件已略去).图示关系中未涉及到的基本反应类型为置换反应;化学方程式①为CaCO3+2HCl═CaCl2+H2O+CO2↑; ②为CaO+H2O═Ca(OH)2;B在生产或生活中的一种用途是用作建筑材料.查看答案和解析>>
科目:初中化学 来源: 题型:推断题
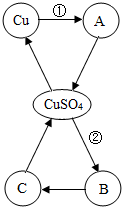 如图是关于铜及其化合物的知识网络图,“→”表示一种物质转化成另一种物质.A、B、C分别是不同类别的铜的化合物,其中A物质为黑色粉末,B物质易溶于水.
如图是关于铜及其化合物的知识网络图,“→”表示一种物质转化成另一种物质.A、B、C分别是不同类别的铜的化合物,其中A物质为黑色粉末,B物质易溶于水.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 原子、分子都能构成物质 | B. | 原子、分子总是在不断地运动 | ||
| C. | 分子可以再分,原子不能再分 | D. | 原子、分子间都有一定的间隔 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源:2017届湖北省老河口市九年级中考适应性考试化学试卷(解析版) 题型:信息分析题
如图所示A~G是初中化学中常见的物质(反应条件和部分产物已省略,“—”表示相互能反应,“→”表示转化关系),其中A是人体胃液中含有的酸,B与C的组成元素相同,D是一种红色粉末,F是相对分子质量最小的氧化物.请回答下列问题.
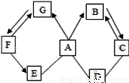
(1)写出物质E的一种用途:_______;
(2)A~G七种物质中,氧化物有_______种;
(3)F→E的反应现象是______________;
(4)C﹣D反应的化学方程式是:______________。
查看答案和解析>>
科目:初中化学 来源:2017届湖北省老河口市九年级中考适应性考试化学试卷(解析版) 题型:选择填充题
下表列出了除去物质中所含少量杂质的方法,其中正确的是
选项 | 物质 | 所含杂质 | 除去杂质的方法 |
A | N2 | O2 | 将气体缓缓通过足量的灼热焦炭 |
B | CaO | CaCO3 | 加水溶解、过滤 |
C | Fe | Zn | 加入过量的稀盐酸,过滤,洗涤,干燥 |
D | FeCl2溶液 | CuCl2溶液 | 加入过量的铁粉, 过滤 |
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
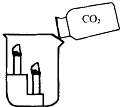 点燃两支蜡烛,分别放在白铁皮架的两个阶梯上,把白铁皮架放在烧杯里(如图所示).沿烧杯内壁缓缓倾倒二氧化碳.
点燃两支蜡烛,分别放在白铁皮架的两个阶梯上,把白铁皮架放在烧杯里(如图所示).沿烧杯内壁缓缓倾倒二氧化碳.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
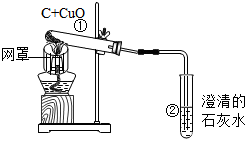 某学习小组同学用如图装置探究木炭还原氧化铜的过程
某学习小组同学用如图装置探究木炭还原氧化铜的过程| 实验操作 | 实验现象 | 实验结论 |
| 取少量的红色固体,置于烧杯中,向其中加入足量稀硫酸,充分搅拌,静置. | 无色溶液变成蓝色 | 猜想成立 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com