
| 化合物 | M1 | M2 | M3 |
| 相对分子质量 | 180 | 60 | 16 |
| A% | 40% | 40% | 75% |
| A. | 72 | B. | 36 | C. | 24 | D. | 12 |
分析 假设M1、M2、M3的分子中分别含有x、y、z个R原子,R的相对原子质量为a,然后结合M1、M2、M3的相对分子质量和M1、M2、M3为三种化合物中R元素的质量分数求出M1、M2、M3的分子中R元素原子的个数比,然后假设M3中R原子个数为1,求出R的相对原子质量,代入其余两种化合物的R元素的质量分数的求解公式求出R元素的质量分数看是否符合要求即可解答.
解答 解:设M1、M2、M3的分子中分别含有x、y、z个R原子,R的相对原子质量为a,则$\frac{xa}{16}$×100%=75%;$\frac{ya}{60}$×100%=40%;$\frac{za}{180}$×100%=40%,所以x:y:z=1:2:6.
假设M1中有1个R原子,则M1中R元素的质量分数为:$\frac{xa}{16}$×100%=75%,a=12;然后M1、M2、M3的分子中R原子的个数比是1:2:6,M1中含有1个R原子,则M2中含有2个,M3中含有6个,故M3中R元素的质量分数为$\frac{6×12}{180}$×100%=40%,
M2中R元素的质量分数为$\frac{2×12}{60}$×100%=40%,都符合要求,
所以R的相对原子质量为12,
故选:D.
点评 本题是在知道相对原子质量和某种元素在化合物中的质量分数确定化学式的题,从根据化学式计算化合物中元素的质量分数入手,采用假设的思想解答.


科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 在蒸馏水中滴加紫色石蕊试液,观察,颜色没有变化 | |
| B. | 加水稀释后测盐酸溶液pH,pH变大 | |
| C. | 在食盐水中滴加紫色石蕊试液,观察,颜色没有变化 | |
| D. | 在稀盐酸中滴加紫色石蕊试液,观察,石蕊变红 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
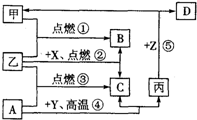 如图所示是初中化学中常见物质间的转化关系,其中甲、乙为气态单质,丙为固态单质;A、B、C均为氧化物,常温下B为液态,化合物D的水溶液呈浅绿色.
如图所示是初中化学中常见物质间的转化关系,其中甲、乙为气态单质,丙为固态单质;A、B、C均为氧化物,常温下B为液态,化合物D的水溶液呈浅绿色.查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com