
 CaCO3↓+CO2↑+H2O,得到沉淀1.0g.回答下列问题:
CaCO3↓+CO2↑+H2O,得到沉淀1.0g.回答下列问题: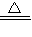 CaCO3↓+CO2↑+H2O
CaCO3↓+CO2↑+H2O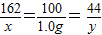


科目:初中化学 来源: 题型:
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
查看答案和解析>>
科目:初中化学 来源:2012年初中毕业升学考试(四川乐山卷)化学(带解析) 题型:计算题
取只含碳酸氢钙的硬水a g,充分加热,发生如下反应:
Ca(HCO3)2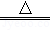 CaCO3↓+CO2↑+H2O,得到沉淀1.0g.回答下列问题:
CaCO3↓+CO2↑+H2O,得到沉淀1.0g.回答下列问题:
(1)碳酸氢钙中钙元素与氧元素的质量比为 。
(2)计算此硬水中碳酸氢钙的质量是多少?
(3)将a g这样的硬水充分煮沸,理论上可得到的软水质量为 。
查看答案和解析>>
科目:初中化学 来源:2012年初中毕业升学考试(四川乐山卷)化学(解析版) 题型:计算题
取只含碳酸氢钙的硬水a g,充分加热,发生如下反应:
Ca(HCO3)2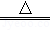 CaCO3↓+CO2↑+H2O,得到沉淀1.0g.回答下列问题:
CaCO3↓+CO2↑+H2O,得到沉淀1.0g.回答下列问题:
(1)碳酸氢钙中钙元素与氧元素的质量比为 。
(2)计算此硬水中碳酸氢钙的质量是多少?
(3)将a g这样的硬水充分煮沸,理论上可得到的软水质量为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com