
【题目】酸和碱是初中化学重要的化合物
⑴将①浓盐酸、②浓硫酸、③NaOH 溶液、④Ca(OH)2 溶液、⑤NaCl 溶液分别敞口放置在空气 中,一段时间后,溶液质量增加的是______(填序号).
⑵欲将 50g 溶质质量质量分数为 98%的浓硫酸稀释成 19.6%的稀盐酸,需要加水_____g,请 简述稀释浓硫酸的正确操作.____________
⑶用 NaOH 固体配制 50g 质量分数为 10%的 NaOH 溶液制作“叶脉书签”,所需的玻璃仪器 有___________,量取水时若仰视读数,会使得到的溶液中溶质质量分数____________(填“偏大”、“偏小”或“不变”)
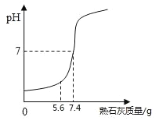
⑷为中和实验后废液中含有的盐酸,取 100g 废液向其中加入熟石灰,反应过程中溶液的 pH 随加入熟石灰质量的变化关系如图所示.
①请根据图示计算废液中盐酸的质量分数____________.
②当加入 5.6g 熟石灰时,溶液中的溶质有______,若改用 7.4g 氢氧化钠与相同量的废液反 应,反应后所得溶液的 pH______7(填“>”,“<”或“=”).
【答案】 ②③ 200 将浓硫酸沿着烧杯壁缓缓倒入到水中,同时用玻璃棒不断搅拌. 烧杯,玻璃棒,量筒,胶头滴管; 偏小 7.3% CaCl2、HCl <
【解析】
(1)浓盐酸具有挥发性,敞口放置一段时间溶液的质量会减少,浓硫酸具有吸水性,敞口放置一段时间溶液的质量会增加,氢氧化钠能和空气中的二氧化碳反应生成碳酸钠和水,溶液的质量会增加,氢氧化钙能和空气中的二氧化碳反应生成碳酸钙沉淀和水,溶液的质量会减少,氯化钠溶液敞口放置一段时间溶液的质量无明显变化,所以溶液质量增加的是②③;(2)浓硫酸的在稀释的过程中溶质的质量没有发生改变,假设稀释之后溶液的质量为x,则有![]() ,
,![]() ,所以加入水的质量为
,所以加入水的质量为![]() ,稀释浓硫酸的正确操作是将浓硫酸沿着烧杯壁缓缓倒入到水中,同时用玻璃棒不断搅拌;(3)配制溶液所需要的玻璃仪器有烧杯、玻璃棒、量筒和胶头滴管,用量筒量取液体仰视读数会使量取的水偏多,则溶质的质量分数偏小;(4)当加入7.4g氢氧化钙时恰好完全反应,根据氢氧化钙的质量和反应的化学方程式可以求出盐酸的质量分数。
,稀释浓硫酸的正确操作是将浓硫酸沿着烧杯壁缓缓倒入到水中,同时用玻璃棒不断搅拌;(3)配制溶液所需要的玻璃仪器有烧杯、玻璃棒、量筒和胶头滴管,用量筒量取液体仰视读数会使量取的水偏多,则溶质的质量分数偏小;(4)当加入7.4g氢氧化钙时恰好完全反应,根据氢氧化钙的质量和反应的化学方程式可以求出盐酸的质量分数。
解:设废液中盐酸的质量为x
2HCl+Ca(OH)2=CaCl2+2H2O
73 74
x 7.4g
![]()
![]()
![]()
答:废液中盐酸的质量分数为7.3%。
当加入5.6g熟石灰时溶液中发生了2HCl+Ca(OH)2=CaCl2+2H2O的反应,所以溶液中的溶质有CaCl2和没有反应完的HCl,若改用氢氧化钠和相同的废液反应,则中和同样的盐酸需要氢氧化钠的质量为8g,加入7.4g氢氧化钠不能把所有的盐酸中和,盐酸有剩余,所以溶液呈酸性,溶液的pH小于7。


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】元素周期表是学习和研究化学的重要工具,可以从表中获得许多知识。图A(见下表)是元素周期表的一部分;图B和图C 是元素周期表中两种元素的原子结构示意图。请你根据图表回答下列问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
第二 周期 | 3 Li 锂 7 | 4 Be 铍 9 | …… | 5 B 硼 11 | ① | 7 N 氮 14 | 8 O 氧 16 | 9 F 氟 19 | 10 Ne 氖 20 |
第三 周期 | 11 Na 钠 23 | ② | …… | 13 Al 铝 27 | 14 Si 硅 28 | ③ | 16 S 硫 32 | 17 Cl 氯 35.5 | 18 Ar 氩 40 |

(1)从图A中找出原子序数为16的元素名称为_______;
(2)图C是某元素的原子结构示意图,该原子在化学反应中易______电子;
(3)图B是某元素的原子结构示意图,该元素在图A中的位置是______(选填①、②或③)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】元素周期表是化学学习的重要工具,依据下表回答问题:
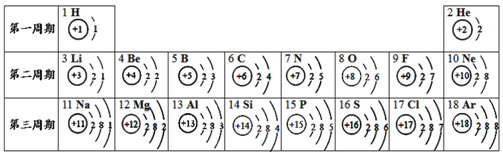
(1)表中14号元素的化学性质与_____________元素相似;
(2)通过上表的分析可知:元素所在的周期数=该元素原子核外的_____________;
(3)在化学反应中,铝原子失电子形成铝离子,写出铝离子符号_____________;
(4)钠元素与氧元素形成的化合物化学式为_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某实验小组的同学在学习了初中化学后,发现课本上对二氧化碳的收集方法是矛盾的。如验证呼出气体和吸入气体中二氧化碳的含量时,可以用排水法收集呼出的气体,但是实验室制取二氧化碳时,又说二氧化碳不能用排水法收集,原因是___________________。那么二氧化碳能否用排水法收集呢?同学们就此展开探究。
实验一:制取二氧化碳,用石灰石与稀盐酸反应,该反应的化学方程式为_____________;分别用向上排空气法和排水集气法收集两瓶气体并分别标注为①和②。
实验二:将两瓶气体分别倒立于盛有足量氢氧化钠溶液的玻璃水槽中。一段时间后,①号集气瓶中的溶液的体积约为集气瓶容积的4/5,②号集气瓶中的溶液几乎全充满。结论是_____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列各组物质,能相互反应且反应前后溶液总质量增加的是( )
A. 氯化钡溶液和稀硫酸 B. 硝酸钾溶液和硫酸镁溶液
C. 碳酸钠固体和稀盐酸 D. 铁和硫酸铜溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图中A、B、C、D是四种常见的物质。其中,A是胃酸的主要成分,B为最轻的气体,C属于盐类,是用小苏打治疗胃酸过多症时发生反应的生成物之一,D的溶液呈黄色。
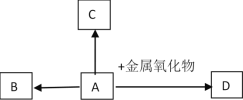
(1)C物质的化学式是__________。
(2)写出符合下列转化的化学反应方程式:
A→B:____________________________(只写一个)
A→D:_______________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】肼(N2H4)是氮和氢形成的化合物,易溶于水。工业上利用尿素法生产肼,同时得副产品十水碳酸钠,工艺流程如下:
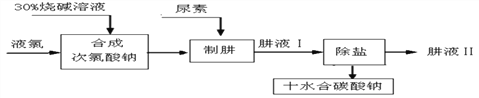
(资料)①尿素的化学式为CO(NH2)2; ②Cl2+H2O==HCl+HClO;
③制肼过程的反应为CO(NH2)2+NaClO+2NaOH==N2H4+Na2CO3+NaCl+H2O;
下列说法不正确的是
A. 尿素不能与熟石灰、草木灰等碱性物质混合使用,会生成氨气,造成肥效流失
B. Cl2与NaOH溶液发生反应的化学方程式为Cl2+2NaOH==NaCl+NaClO+H2O
C. 从母液中分离出十水合碳酸钠晶体,可采用蒸发浓缩、冷却结晶、过滤、洗涤干燥等步骤
D. 从后续反应过程来看,若要使原料利用率最佳,合成次氯酸钠时投入的液氯与烧碱的质量之比为71 :80
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】从微观的角度了解物质及其变化,有助于更好地认识物质的组成和变化的本质。
(1)下表为部分元素的原子结构示意图
元素名称 | 氢 | 氦 | 氧 | 氟 | 钠 | 硫 |
元素符号 | H | He | O | F | Na | S |
原子结构示意图 |
|
|
|
|
|
|
①表中氧原子的核电荷数x=_____
②元素在周期表中的周期序数等于该元素原子具有的电子层数。上表所列的6种元素中,位于第一周期的元素有_____种。
③氟原子得到一个电子所形成离子的离子符号为_____。
④由上表中两种元素组成的一种化合物排放到空气中会形成酸雨,该化合物为_____。
(2)如图为金属钠与水反应的示意图
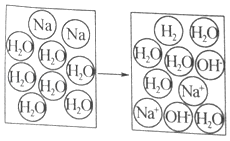
①保持水的化学性质的最小粒子是_____。
②写出该反应的化学方程式:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一种管道疏通剂,主要成分为铝粉和氢氧化钠混合粉末。已知:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,小勇利用如图装置测定疏通剂中铝的质量分数。
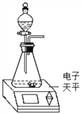
Ⅰ.取样品20g,倒入容积为200mL的锥形瓶中,然后在分液漏斗中加入水,置于电子天平上测出总质量m1。
Ⅱ.打开活塞,加入足量的水充分反应,直到没有固体剩余,静置一段时间,测出总质量m2。实验数据如下表:
反应前总质量m1 | 反应后总质量m2 |
371.84g | 371.24g |
回答下列问题:
(1)请计算样品中铝的质量分数是____;
(2)以下情形会导致样品中铝的质量分数测量结果偏低的是____(填字母序号)。
A.实验装置漏气
B. 在反应过程中有水蒸气逸出
C.向锥形瓶中倒入样品时,撒出了部分粉末
D.没有等装置中氢气全部排尽就称量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com