
分析 氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,剩余固体物质10.0g为生成氯化钾和二氧化锰的混合物;由质量守恒定律,混合物减少的质量即为生成氧气的质量,由反应的化学方程式列式计算出参加反应的氯酸钾的质量,进而计算出混合物中二氧化锰的质量分数.
解答 解:(1)由质量守恒定律,生成氧气的质量为14.8g-10g=4.8g.
(2)设参加反应的氯酸钾的质量为x
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 96
x 4.8g
$\frac{245}{96}=\frac{x}{4.8g}$ x=12.25g
混合物中二氧化锰的质量分数为$\frac{14.8g-12.25g}{14.8g}×$100%≈17.2%.
答:(1)4.8g;(2)混合物中二氧化锰的质量分数为17.2%.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出氧气的质量是正确解答本题的前提和关键.


科目:初中化学 来源: 题型:选择题
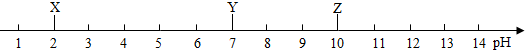
| A. | X是稀盐酸 | B. | Y是食盐水 | C. | Z是石灰水 | D. | 以上说法都不对 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
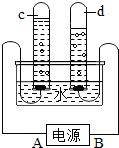 电解水的实验装置如图所示,根据图回答:
电解水的实验装置如图所示,根据图回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
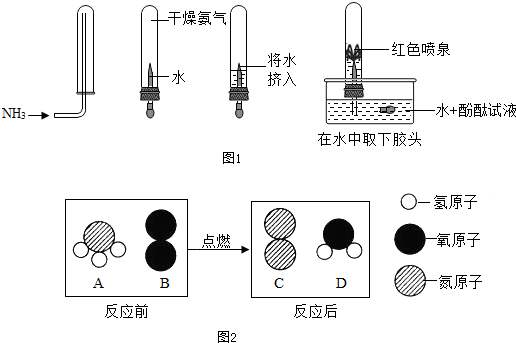
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
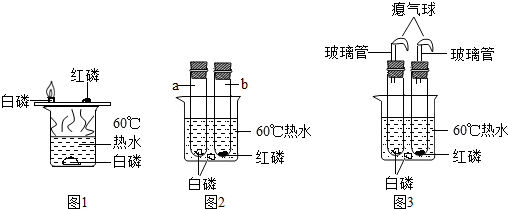
| 现象 | 解释 |
| a.试管中白磷燃烧,热水 中白磷没有燃烧. b.试管中红磷没有燃烧. | 试管中红磷、热水中自磷都没有燃烧的原因是 ①: ②. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com