
| A、H2SO4、Na2SO4 、BaCl2 、AlCl3 |
| B、BaCl2 、CuCl2 、NaNO3、Na2SO4 |
| C、H2SO4、NaOH、MgCl2、Ba(NO3)2 |
| D、Na2CO3、HCl、CaCl2、(NH4)2CO3 |


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
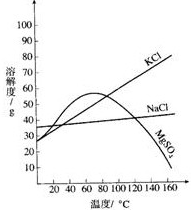 如图是氯化钾、氯化钠、硫酸镁三种物质的溶解度曲线.
如图是氯化钾、氯化钠、硫酸镁三种物质的溶解度曲线.查看答案和解析>>
科目:初中化学 来源: 题型:
| A、把胶头滴管伸入试管中滴加液体 |
| B、在托盘天平上直接称量固体物质 |
| C、用药匙或纸槽把粉末药品送入试管底部 |
| D、握住试管夹的短柄给试管内的药品加热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com