配制980g 20%的稀硫酸需98%(密度为1.84g/cm3)的浓硫酸______mL,水______mL.
【答案】
分析:设出浓硫酸的体积,利用m=ρV可计算溶液的质量,再根据溶液配制前后溶质的质量不变来列式计算,根据稀溶液与浓溶液的质量差来计算水的质量,进一步得到需加水的体积.
解答:解:设需要浓硫酸的体积为V,则
根据浓溶液在配制稀溶液时溶质的质量不变得,
V×1.84g/cm
3×98%=980g×20%
解得V=108.7mL,
水的质量为980g-108.7mL×1.84g/cm
3=780g,
则水的体积为
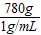
=780mL,
故答案为:108.7mL;780mL.
点评:本题难度不是很大,主要考查了溶质质量分数的有关计算,培养学生的计算能力和理解能力.
