
分析 在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,据此进行分析解答.
解答 解:根据在金属活动性顺序中,镁>锌>氢>铜>银,故锌不能与Mg(NO3)2溶液反应,锌先与硝酸银反应生成银和硝酸锌溶液,硝酸银溶液反应完,若还有锌,再与硝酸铜溶液反应生成铜和硝酸锌溶液.
(1)充分反应过滤,向滤出固体中滴加稀硫酸,若有气泡产生,说明有能与稀硫酸反应的金属存在,这种金属应是锌,说明锌是过量的,则滤出的固体物质中一定有银、铜、锌;滤液中一定有硝酸镁、硝酸锌.
(2)充分反应过滤,向滤出固体中滴加稀硫酸,若无气泡产生,说明滤渣中的金属不与稀硫酸反应,则可能是锌只与硝酸银反应生成银和硝酸锌溶液,也可能是锌与硝酸银、硝酸铜均发生了反应(可能与硝酸铜溶液只反应了一部分,或恰好完全反应),但一定没有锌剩余,则滤出的固体物质中一定有银,可能含有铜;滤液中一定有生成的硝酸锌、没有参加反应的Mg(NO3)2,可能含有硝酸银和硝酸铜.
故答案为:(1)银、铜、锌;硝酸镁、硝酸锌;
(2)银;铜;硝酸镁、硝酸锌;硝酸银和硝酸铜.
点评 本题难度不是很大,熟练掌握金属的化学性质、综合考虑各种出现的情况是正确解答此类题的关键.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 实验目的 | 所用试剂或方法 |
| A | 除去NaCl溶液中少量Na2CO3 | 适量澄清石灰水、过滤 |
| B | 除去二氧化碳中混有的水蒸气 | 通入装有生石灰的干燥管 |
| C | 从高锰酸钾制氧气的残余物中分离出MnO2 | 加水溶解、过滤、洗涤、干燥 |
| D | 区分失去标签的稀盐酸和稀硫酸 | 紫色石蕊溶液或铁粉 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 |  |  | 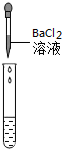 |
| 实验现象 | 试纸变色,对比标准比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 |
| 加入稀硫酸的质量(g) | 10 | 10 | 10 | 10 | 10 | 10 |
| 剩余固体的质量 (g) | 9.35 | 8.70 | 8.05 | 7.40 | 6.75 | 6.75 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
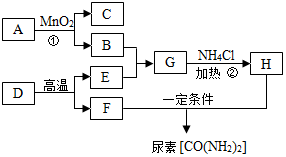 如图表示某些物质间转化关系.A、B为组成元素相同的无色液体,D是大理石的主要成分,C、F、H为气体,且H有刺激性气味.
如图表示某些物质间转化关系.A、B为组成元素相同的无色液体,D是大理石的主要成分,C、F、H为气体,且H有刺激性气味.查看答案和解析>>
科目:初中化学 来源: 题型:解答题



查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前(%) | 70 | 14 | m | 10 |
| 反应后(%) | 42 | n | 40 | 10 |
| A. | 若消耗3 g乙,则生成17 g丙 | |
| B. | 丙可能是单质 | |
| C. | 丁一定是该反应的催化剂 | |
| D. | 甲、乙的质量之和一定等于生成丙的质量 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 离子都带有电荷,所以带有电荷的粒子一定是离子 | |
| B. | 不同种分子构成混合物,所以混合物一定有不同种分子构成 | |
| C. | 单质只含有一种元素,所以由一种元素组成的纯净物一定是单质 | |
| D. | 化合反应生成一种物质,所以生成一种物质的反应一定是化合反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com