
【题目】下图是常见固体物质的溶解度曲线,根据图示回答:
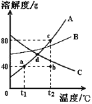
(1)对A物质来说,a点的意义是_____________________________。
(2)将t1℃140 g A的饱和溶液升温至t2℃时,此时溶液是______(填“饱和”或“不饱和”)状态,然后再加入A物质40 g,可用曲线上的____点表示。
(3)t2℃时A、B、C三种物质饱和溶液的质量分数由大到小的顺序是______
(4)若将d点对应温度下A、B、C三种物质的饱和溶液降温至t1℃,没有晶体析出的是_______物质。
【答案】t1℃时,A物质的溶解度是40g 不饱和 c A>B>C C
【解析】
(1)通过分析溶解度曲线可知,对A物质来说,a点的意义是:t1℃时,A物质的溶解度是40g;
(2)t1℃时,A物质的溶解度是40g,A物质的溶解度随温度的升高而增大,所以将t1℃140g A的饱和溶液升温至t2℃时,此时溶液是不饱和状态;然后再加入A物质40g,溶质质量变成80g,可用曲线上的c点表示;
(3)t2℃时,A物质的溶解度最大,B物质的溶解度次之,C物质的溶解度最小,所以A、B、C三种物质饱和溶液的质量分数由大到小的顺序是:A>B>C;
(4)C物质的溶解度随温度的降低而增大,所以若将d点温度下A、B、C三种物质的饱和溶液降温至t1℃,没有晶体析出的是C物质;


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】有一包白色粉末,可能由CuSO4、Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种组成。为探究其组成,同学们查阅资料得知NaCl、BaCl2溶液呈中性,经过思考设计并进行了以下实验:
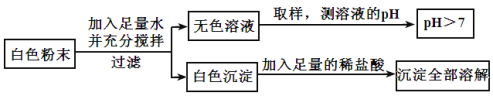
(1)白色粉末中一定不含_____________;可能含有____________。
(2)为最终确定白色粉末的组成,还需要对无色滤液中呈碱性的物质进行探究。
(提出问题)无色滤液中呈碱性的物质是什么?
(作出猜想)猜想Ⅰ:Na2CO3
猜想Ⅱ:NaOH
猜想Ⅲ:Na2CO3和NaOH
(进行实验)
实验步骤 | 实验现象 | 实验结论 |
① 取无色滤液少许于试管中,滴加过量的BaCl2溶液 | ________ | 猜想Ⅱ不成立 |
② 在①反应后的试管中滴加________ | 溶液变为红色 | 猜想Ⅲ成立 |
(得出结论)白色粉末的成分是________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙两种固体物质的溶解度曲线图,请回答下列问题:
 。
。
(1)20℃时,将15g的甲物质充分溶解在50g水中,所形成溶液的溶质质量分数是 .
(2)10℃时,欲将150g乙物质的饱和溶液质量分数减小一半,需要加水 g.
(3)某同学欲将20℃时300g20%的甲溶液溶质质量分数增大一倍.他采用恒温蒸发水的方法,并进行了如下计算:
解:设蒸发水的质量为x,
300g×20%=x×40%解得:x=150g。试分析:他能否达到目的,并说明理由。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】南昌大学研发的“硅衬底高光效GaN基蓝色发光二极管技术”获得国家技术发明一等奖。请回答下列问题:
(1)下图是镓在元素周期表中的信息以及原子结构示意图,镓属于_______元素,相对原子质量为______;下列原子结构示意图所对应的元素与镓元素的化学性质相似的是_______(填序号);
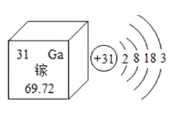
A 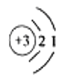 B
B  C
C  D
D 
(2)GaCl3中镓元素的化合价为______。
(3)传统制备氮化镓的化学原理是:![]() ,其中X的化学式为______。
,其中X的化学式为______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示为A、B、C三种固体物质的溶解度曲线,下列有关说法正确的是(_______)
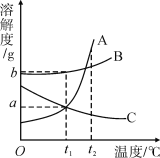
A.t2 ℃时三种物质的饱和溶液中,溶质质量最大的是A
B.将t1 ℃时,A、B、C三种物质的饱和溶液,分别蒸发等量的水后温度恢复至t1 ℃,析出溶质的质量关系为B>A=C
C.可用降低温度的方法使t2 ℃时C的不饱和溶液变为饱和溶液
D.将t2 ℃时三种物质的饱和溶液降温至t1 ℃时,溶质的质量分数由大到小的顺序是______________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,某兴趣小组在进行酸碱中和反应的实验探究时,向烧杯中氢氧化钠溶液中滴加稀盐酸一会儿后,发现忘记滴加指示剂,甲同学从烧杯中取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞溶液,振荡,观察到酚酞溶液不变色。
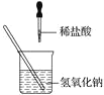
请写出该中和反应方程式:___________________________________________________。
(1)猜想与假设:
猜想一:甲同学:“两种物质已恰好完全中和,溶液呈中性”;
猜想二:乙同学:“反应后氢氧化钠过量,溶液呈碱性”;
猜想三:丙同学:__________________________________________________________。
甲、丙两位同学经过讨论后觉得乙同学的猜想不正确,两位同学的理由是:_______________________。
(2)设计并进行实验:
①为了验证自己的猜想,甲同学设计了以下实验方案:
实验步骤 | 实验现象 | 实验结论 |
用洁净干燥的玻璃棒蘸取少量反应后的溶液滴在干燥的pH试纸上,观察颜色变化并与标准比色卡对比。 | pH________(填“>”“=”或“<”)7 | 猜想一不成立 |
②请你设计另一个实验(与甲同学方案不同)方案,验证丙同学的猜想,并填写下表:
实验步骤 | 实验现象 | 实验结论 |
__________ | __________ | __________ |
(3)拓展探究:你还能设计不同的实验方案来验证丙同学的猜想吗?
实验步骤 | 实验现象 | 实验结论 |
__________ | __________ | __________ |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】许多物质在溶液中都以离子形式存在。我们熟悉的复分解反应就是溶液中离子间结合得到水、气体或沉淀的一类化学反应。如:氢氧化钠与盐酸的反应就是溶液中的H+和OH-结合成水分子的过程。结合以上信息,你认为下列各组离子间不能反应的是( )
A. H+、Na+、OH-、![]()
B. Na+、K+、Cl-、OH-
C. H+、K+、![]() 、
、![]()
D. K+、Ba2+、Cl-、![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】从海水中制备纯碱和金属镁的流程如下图所示:下列说法错误的是
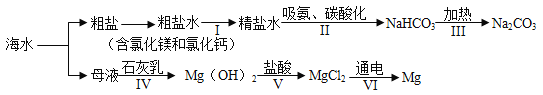
A. 流程I依次向粗盐水中加入过量Ca(OH)2溶液、Na2CO3溶液和适量稀盐酸去除杂质
B. 流程II吸氨是使溶液呈碱性,有利于吸收二氧化碳
C. 流程IV、V是通过化学方法富集氯化镁
D. 上述流程涉及到三种基本反应类型
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学研究性学习小组同学取 10g 石灰石样品,用足量的稀盐酸测定石灰石中碳酸钙的质量分数(假设石灰石中杂质不与盐酸反应)。测量 5 分钟内生成 CO2 质量的数据如下表:
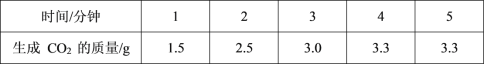
请回答下列问题:
I.石灰石中的 CaCO3 完全反应时,生成二氧化碳气体的物质的量为_____mol。
II.该石灰石中 CaCO3 的质量分数是多少_______?(根据化学方程式列式计算)
III.请根据表中数据分析,你能发现数据背后的化学反应规律是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com