
����Ŀ����һ��������a��b��c��d�������ʷ���һ�ܱ������У���һ�������·�Ӧһ��ʱ���÷�Ӧ������ʵ��������£�����˵������ȷ���ǣ� ��
���� | a | b | c | d |
��Ӧǰ����/g | 6.4 | 3.2 | 4.0 | 0.5 |
��Ӧ������/g | ���� | 2.56 | 7.2 | 0.5 |
��a��b�Ƿ�Ӧ�dһ���Ǵ���
�ڷ�Ӧ��a���ʵ�������3.84g
��c������Ԫ�ص����࣬һ����a��b����������Ԫ�ص�����֮��
����a��b����Է�������֮����2��1����Ӧ��a��b�Ļ�ѧ������֮����1��1��
A.�٢�
B.�ڢ�
C.�ڢ�
D.�٢ڢ�
���𰸡�B
���������⣺���������غ㶨�ɣ��ɱ������ݿ�֪��b������������3.2g��2.56g=0.64g����ȷ��b�Ƿ�Ӧ�c������������7.2g��4.0g=3.2g����ȷ��c�������d��������Ӧǰ�䣬�����Ǵ���Ҳ���ܲ��μӷ�Ӧ�� �� �μӷ�Ӧ��b������Ϊ0.64g��������c��������3.2g���������غ㶨�ɣ�aӦ�Ƿ�Ӧ��Ҳμӷ�Ӧ��a������Ϊ3.2g��0.64g=2.56g��d���������䣬d�������÷�Ӧ�Ĵ�����Ҳ����û�вμӷ�Ӧ���ʴ����ڸ��ݷ�����aӦ�Ƿ�Ӧ��Ҳμӷ�Ӧ��a������Ϊ3.2g��0.64g=2.56g���ʴ������ֵΪ6.4g��2.56g=3.84g���ʶԣ��۸���ǰ�ߵķ�����֪��a��b�Ƿ�Ӧ�c����������Ը÷�Ӧ���ڻ��Ϸ�Ӧ��c������Ԫ�ص����࣬һ����a��b����������Ԫ�ص�����֮�ͣ��ʶԣ�������A������B����Է�������֮��Ϊ2��1���跴Ӧ��A��B�Ļ�ѧ������֮��Ϊx��y���������ʵ���Է�����������ǰ��Ļ�ѧ������֮�ȵ��ڲμӷ�Ӧ�����ʵ�����֮�ȣ� ![]() ����ã�x��y=2��1���ʲ���ȷ��
����ã�x��y=2��1���ʲ���ȷ��
��ѡB��
�����㾫����������Ĺؼ���������������ص�������õ����֪ʶ�����մ�������ý�����ڻ�ѧ��Ӧ���ܸı��������ʵĻ�ѧ��Ӧ���ʣ��������������ͻ�ѧ�����ڷ�Ӧǰ��û�з����仯�����ʣ���һ�������䣩�����ڻ�ѧ��Ӧ����������ýд����ã��Լ��������غ㶨�ɼ���Ӧ�õ����⣬�˽�������غ㶨��ֻ�����ڻ�ѧ�仯���������������仯���ڲ��μӷ�Ӧ����������������������������������ܼ��롰�ܺ͡��У���Ҫ���ǿ����е������Ƿ�μӷ�Ӧ�����ʣ������壩������©��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ζ����彡����Σ������Խ��Խ�ܵ���ѧ������ӣ��������ƾ�����ζ�������ʳ�ηdz����ƣ����������Ƶ�ˮ��Һ�Լ��ԣ�ʳ�ε�ˮ��Һ�����ԣ������������ֵ���������������������Һ��ʳ����Һѡ�õ��Լ�Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ�����ݰ����ʽ��з��࣬���о����ʵ���ɡ��ṹ�����ʺ���;�ij��÷����������������ʣ�
�ٰơ���������ˮ�����ף���ˮ����������Ӳ������ͭ���۵��������ס�þ�����ɱ���
ÿ���о���һ�����ʵ�������������ֲ�ͬ������������������(����)
A. ���ס�������þ�� B. ���ס�ˮ����þ��
C. ���ס�ˮ�����ɱ� D. ��������ͭ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�������ȷ���ǣ� ��
A.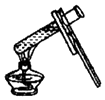 ����Һ��
����Һ��
B.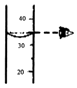 ����Һ�����
����Һ�����
C.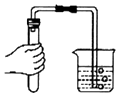 ���������
���������
D.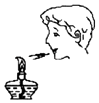 Ϩ��ƾ���
Ϩ��ƾ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݳ���Ԫ�صĻ��ϼۣ��������ʵĻ�ѧʽ�������ڣ���д������ǣ� ��
A. ����þ��MgO�� B. �Ȼ�����AICI3�� C. ��������Fe2��SO4)3 D. �����ƣ�Na2O��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ���ӳ��׳�Ƶ�ʹ����������������м�����ĺ������������������û�ѧ����ʽ��ʾΪ_____����Ӧ�Ļ���������___________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������й㷺��Ӧ�ã�
��1��ͭ�������������ߣ���Ϊ�������õ���չ�Ժ� �� �糵�������Ҫ�������̸֣����������ĺϽ���Ӳ�ȱȴ��� ��
��2����ҵ����һ����̼�ͳ������ڸ������������仯ѧ����ʽΪ����¯�����н�̿�������� ��
��3����ֹ������ʴ�DZ���������Դ����Ч;��֮һ�����з������ܷ�ֹ������ʴ����������ĸ��ţ���
A.����Ƹ�
B.����Ϳ����
C.���ֽ���ʳ��ˮ
D.����ڳ�ʪ�Ŀ�����
��4������ʯ�ڹ�ҵ��ȡ�������Ĺ�����������Ҫ�����ã��������ͷ����ƣ�NaF�������������·�Ӧ���ɱ���ʯ��Na3AlF6����ͬʱ�õ������ƣ�д���˷�Ӧ�Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������¶���ڳ�ʪ�Ŀ�����,һ��ʱ���,�����������ӵ���( )
A. Ũ���� B. ���� C. ��ʯ�� D. Ũ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�����������pH=1����Һ�д����������
A. K+��Na+��OH-��SO42- B. K+��Cu2+��SO42-��NO3-
C. Ba2+��Na+��Cl-��SO42- D. Na+��K+��Cl-��CO32-
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com