
在制取氢气的实验中同学们需要用到稀硫酸,现预将50g质量分数为98%,密度为1.84g/cm3的浓硫酸稀释为质量分数为20%的稀硫酸,你认为需取用蒸馏水的体积为
A.106m B.195mL C.245mL D.400.8mL
 备战中考寒假系列答案
备战中考寒假系列答案科目:初中化学 来源: 题型:阅读理解

| ||
| ||
| 物质 | 所需时间 | 价格 |
| 甲金属粒 | 约13900s | 1000g/10.00元 |
| 乙金属粒 | 约50s | 500g/20.00元 |
| 丙金属粒 | 约20s | 25g/10.80元 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| ||
| ||
| ||
| 甲 | 乙 | |
| 实验过程 | 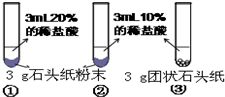 |
 |
| 现象 | 试管①、②、③中产生气泡快慢的顺序为: ①>②>③. |
|
| 分析结论 | Ⅰ碳酸钙与稀盐酸反应的化学方程式为 CaCO3+2HCl═2CaCl2+H2O+CO2↑ CaCO3+2HCl═2CaCl2+H2O+CO2↑ Ⅱ对比甲同学实验①②可知, 盐酸越浓(溶质的质量分数越大) 盐酸越浓(溶质的质量分数越大) ,化学反应的速度越快;Ⅲ对比甲同学实验 ②③ ②③ (填实验序号)可知,反应物的接触面积越大,反应速率越快 快 .Ⅳ乙同学的实验中,数据记录纸上应该连续记录的实验数据是 时间 时间 和锥形瓶及药品的质量或二氧化碳的质量 锥形瓶及药品的质量或二氧化碳的质量 . | |
| 第一份 | 第二份 | 第三份 | 第四份 | |
| 取样品质量(g) | 6.25 | 6.25 | 6.25 | 6.25 |
| 取稀盐酸的体积(mL) | 10.0 | 20.0 | 30.0 | 40.0 |
| 产生气体的质量(g) | 0.88 | 1.76 | 2.20 | m |


查看答案和解析>>
科目:初中化学 来源:2013届江苏省仪征市大仪中学九年级上学期末考试化学试卷(带解析) 题型:探究题
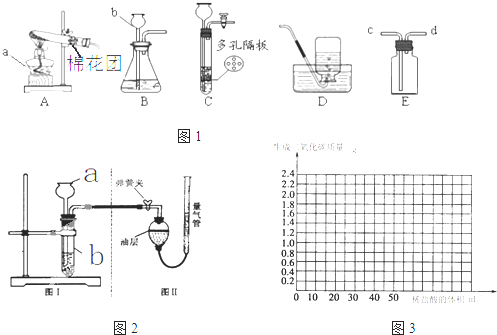
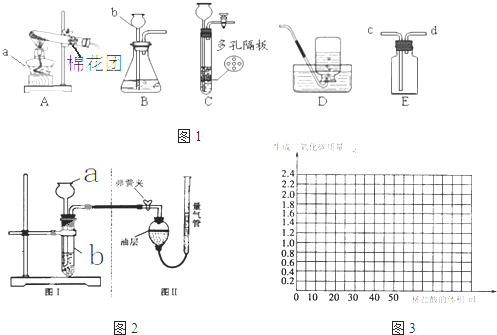
(24分)下图所示为实验室常用的实验装置:
(1)写出下列仪器名称:a ;b 。
(2)实验室用高锰酸钾制取氧气时,应选择的发生装置是 (填装置的字母代号),化学方程式是 ,用双氧水制取氧气的化学方程式为 。
(3)实验室用锌和稀硫酸反应制取氢气的化学方程式是 ,若将E装置中收集的氢气排出,应从 (填c或d)口通入蒸馏水。
(4)装置C相对于装置B在操作方面的优势为 。
A.可以随时加液 B.可以控制反应速率 C.可以控制反应发生与停止
同学们对美术组的环保石头纸(主要成分为碳酸钙,加入适量聚乙烯和少量胶合剂)展开探究:
[拓展实验一] 探究影响石头纸与盐酸反应快慢的因素
(5)甲、乙两同学设计实验如下:
| | 甲 | 乙 |
| 实验过程 |  |  |
| 现象 | 试管①、②、③中产生气泡快慢的顺序为: ①>②>③。 |  |
| 分析结论 | Ⅰ 碳酸钙与稀盐酸反应的化学方程式为 Ⅱ 对比甲同学实验①②可知, ,化学反应的速度越快; Ⅲ 对比甲同学实验 (填实验序号)可知,反应物的接触面积越大,反应速率越。 Ⅳ 乙同学的实验中,数据记录纸上应该连续记录的实验数据是 和 。 | |

| | 第一份 | 第二份 | 第三份 | 第四份 |
| 取样品质量(g) | 6.25 | 6.25 | 6.25 | 6.25 |
| 取稀盐酸的体积(mL) | 10.0 | 20.0 | 30.0 | 40.0 |
| 产生气体的质量(g) | 0.88 | 1.76 | 2.20 | m |

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 甲 | 乙 | |
| 实验过程 |  |  |
| 现象 | 试管①、②、③中产生气泡快慢的顺序为: ①>②>③. | |
| 分析结论 | Ⅰ碳酸钙与稀盐酸反应的化学方程式为______ Ⅱ对比甲同学实验①②可知,______,化学反应的速度越快; Ⅲ对比甲同学实验______(填实验序号)可知,反应物的接触面积越大,反应速率越______. Ⅳ乙同学的实验中,数据记录纸上应该连续记录的实验数据是______ 和______. | |
| 第一份 | 第二份 | 第三份 | 第四份 | |
| 取样品质量(g) | 6.25 | 6.25 | 6.25 | 6.25 |
| 取稀盐酸的体积(mL) | 10.0 | 20.0 | 30.0 | 40.0 |
| 产生气体的质量(g) | 0.88 | 1.76 | 2.20 | m |
查看答案和解析>>
科目:初中化学 来源:不详 题型:问答题
| 甲 | 乙 | |
| 实验过程 | 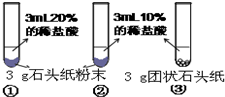 |
 |
| 现象 | 试管①、②、③中产生气泡快慢的顺序为: ①>②>③. |
|
| 分析结论 | Ⅰ碳酸钙与稀盐酸反应的化学方程式为______ Ⅱ对比甲同学实验①②可知,______,化学反应的速度越快; Ⅲ对比甲同学实验______(填实验序号)可知,反应物的接触面积越大,反应速率越______. Ⅳ乙同学的实验中,数据记录纸上应该连续记录的实验数据是______ 和______. | |
| 第一份 | 第二份 | 第三份 | 第四份 | |
| 取样品质量(g) | 6.25 | 6.25 | 6.25 | 6.25 |
| 取稀盐酸的体积(mL) | 10.0 | 20.0 | 30.0 | 40.0 |
| 产生气体的质量(g) | 0.88 | 1.76 | 2.20 | m |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com