
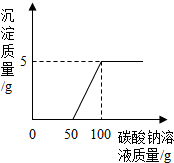
 实验室制取二氧化碳后,将废液过滤,得到含有氯化钙和稀盐酸的混合液,20℃
实验室制取二氧化碳后,将废液过滤,得到含有氯化钙和稀盐酸的混合液,20℃分析 由图象可以看出产生沉淀前消耗50g碳酸钠溶液,这是与废液中盐酸反应的碳酸钠溶液的质量,由于盐酸反应的碳酸钠溶液的质量和质量分数,根据二者反应的化学方程式可以计算出生成氯化钠的质量.由图象中可知生成沉淀的质量,然后依据碳酸钠与氯化钙反应的化学方程式可以计算出生成氯化钠的质量.由两种反应生成的氯化钠的质量和除以所得溶液的质量就得到所得溶液中氯化钠的质量分数,所得溶液的质量应是反应的碳酸钠溶液总质量和混合液141.2g的和减去生成沉淀的质量和生成的二氧化碳的质量.
解答 解:设与盐酸反应时,生成氯化钠的质量为x,生成二氧化碳的质量为y.
Na2CO3+2HCl═2NaCl+CO2↑+H2O
106 117 44
50g×10.6% x y
$\frac{106}{50g×10.6%}=\frac{117}{x}=\frac{44}{y}$
x=5.85g,y=2.2g
设与氯化钙反应时,生成氯化钠的质量为w.
Na2CO3+CaCl2═CaCO3↓+2NaCl
100 117
5g w
$\frac{100}{5g}=\frac{117}{w}$
w=5.85g
所得溶液中氯化钠的质量分数为:$\frac{5.85g+5.85g}{141.2g+100g-2.2g-5g}×100%$=5%
答:所得溶液中氯化钠的质量分数为5%.
点评 本题主要考查含杂质物质的化学方程式计算和溶质质量分数的计算,增加了学生分析问题的思维跨度,考查了学生整合知识的能力,难度较大.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:实验探究题
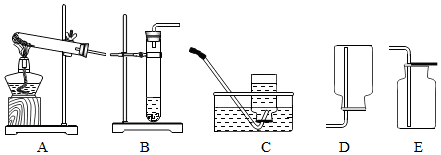
| 装置A | 装置B | |
| 反应状态 | 固体反应生成气体 | 固体和液体反应生成气体 |
| 反应条件 | 加热 | 无需加热 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
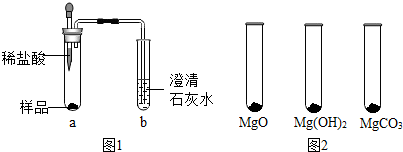
| MgO | Mg(OH)2 | MgCO3 | |
| 消耗稀盐酸的体积/mL | 10.4 | 7.2 | 5.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
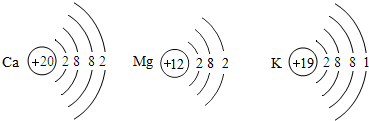
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
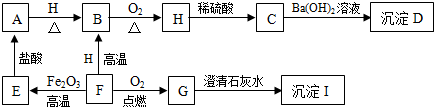
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
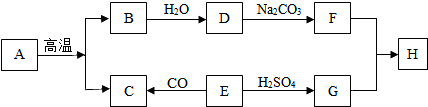
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com