
���� ̼���ƺ�ϡ���ᷴӦ���������ơ�ˮ�Ͷ�����̼�����ݷ�Ӧ�Ļ�ѧ����ʽ�����ṩ�����ݿ��Խ�����ط���ļ�����жϣ�
��� �⣺��1����̼��������Ϊx����������Ϊy����Ӧ��������������Ϊz��
��Ӧ���ɶ�����̼����Ϊ��20g+100g+50g+165.6g=4.4g��
Na2CO3+H2SO4�TNa2SO4+H2O+CO2����
106 98 142 44
x y z 4.4g
$\frac{106}{x}$=$\frac{98}{y}$=$\frac{142}{z}$=$\frac{44}{4.4g}$��
x=10.6g��y=9.8g��z=14.2g��
�μӵ�ϡ���������ʵ���������Ϊ��$\frac{9.8g}{50g}$��100%=19.6%��
�𣺵μӵ�ϡ���������ʵ���������Ϊ19.6%��
��2������Ʒ��Na2CO3����������Ϊ��$\frac{10.6g}{20g}$��100%=53%��
�𣺸���Ʒ��Na2CO3����������Ϊ53%��
��3����Ӧ��������Һ�����ʵ���������Ϊ��$\frac{20g-10.6g+14.2g}{165.6g}$��100%=14.3%��
�𣺷�Ӧ��������Һ�����ʵ�����������14.3%��
���� ������Ҫ����ѧ�����ü��跨�ͻ�ѧ����ʽ���м�����ƶϵ�����������ʱҪע��淶�Ժ�ȷ�ԣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
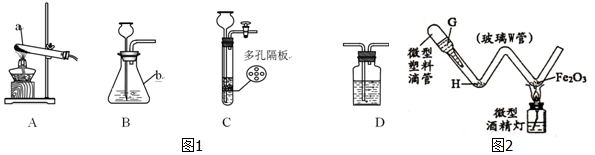
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | �� | �� | �� | �� |
| ���� | ���� | ������� | ��ʯ�� | ���� |
| ��ѧʽ | CH3COOH | KMnO4 | Ca��OH��2 | Na2CO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����һ�ֳ�������������2015��3��23�ս��������У�����¡¡֮�������� �绮��ҹ�գ�����ʮ��׳�ۣ�
����һ�ֳ�������������2015��3��23�ս��������У�����¡¡֮�������� �绮��ҹ�գ�����ʮ��׳�ۣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
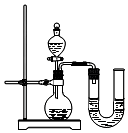 ij��ȤС��Ϊ֤������������Һ��ϡ���ᷢ�����кͷ�Ӧ���Ӳ�ͬ�Ƕ����������ʵ�鷽����������ʵ�飮
ij��ȤС��Ϊ֤������������Һ��ϡ���ᷢ�����кͷ�Ӧ���Ӳ�ͬ�Ƕ����������ʵ�鷽����������ʵ�飮| ��� | ���� | NaOH��Һ | ��t/�� |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | X |
| 3 | 7.30% | 8.00% | 1��4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
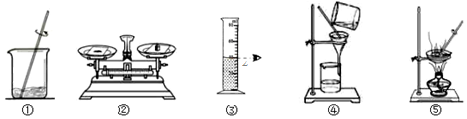
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com