
【题目】海洋是巨大的资源宝库、国防金属﹣﹣镁,就是利用海水制取的.工业上从海水中提取单质镁的过程如图1所示: 
(1)在上述转化过程中发生中和反应的步骤是(填序号).
(2)海水中本身就含有氯化镁,请分析①、②两步再得到氯化镁的目的是 .
(3)小明同学在实验室中用NaOH溶液替代石灰乳模拟生产过程中的第①步,他取NaCl和MgCl2的固体混合物25g,加入适量水完全溶解后,与溶质质量分数为20%的NaOH溶液混合充分反应,记录生成的沉淀与加入NaOH溶液质量关系如图2所示: ①当滴入上述NaOH溶液至图中B点时,烧杯中溶液里含有的溶质为(写化学式).
②当滴入上述NaOH溶液80g时,试通过计算,求此时烧杯中所得不饱和溶液中溶质的质量(计算结果精确至0.1g).
【答案】
(1)②
(2)富集镁元素
(3)NaCl、NaOH;恰好反应时反应的氢氧化钠的质量为:80g×20%=16g 设混合物中MgCl2的质量为x,反应生成NaCl的质量为y
MgCl2+ | 2NaOH═Mg(OH)2↓+ | 2NaCl |
95 | 80 | 117 |
x | 16g | y |
![]() ?? 解得:x=19g,y=23.4g所以,杯中所得不饱和溶液中溶质的质量是:(25g﹣19g)+23.4g=29.4g.答:烧杯中所得不饱和溶液中溶质的质量为29.4g.
?? 解得:x=19g,y=23.4g所以,杯中所得不饱和溶液中溶质的质量是:(25g﹣19g)+23.4g=29.4g.答:烧杯中所得不饱和溶液中溶质的质量为29.4g.
【解析】解:(1)由反应的流程可知,在②中氢氧化镁与盐酸的反应属于酸与碱发生的中和反应;(2)海水或卤水均含有氯化镁,氯化镁溶解在海水中,不能直接提取出来,经过①、②两个步骤将海水中的镁离子提取出来,得到纯净的氯化镁,然后电解才能得到镁.(3)①根据曲线可知,当滴入80gNaOH溶液时,MgCl2完全反应,生成氯化钠和氢氧化镁沉淀,当滴入上述NaOH溶液至图中B点时,氢氧化钠是过量的,溶液中的溶质是:NaCl、NaOH;
故答为:(1)②;(2)富集镁元素;(3)①NaCl、NaOH;
【考点精析】通过灵活运用中和反应及其应用和根据化学反应方程式的计算,掌握中和反应:酸与碱作用生成盐和水的反应;各物质间质量比=系数×相对分子质量之比即可以解答此题.


 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:初中化学 来源: 题型:
【题目】水在生活、生产和化学实验中起着十分重要的作用.
(1)水的净化.向浑浊的天然水中加入明矾,可以加速泥沙的沉降,静置一段时间后,取上层液体过滤,得到略带颜色的液体,实验中,过滤操作中要用到的玻璃仪器有烧杯、玻璃棒和漏斗,其中玻璃棒的作用是 .
(2)水的组成,用如图1实验装置可以证明水的组成,检验a处气体的方法是 . 
(3)水的用途,水是常用的溶剂,如图2为甲、乙、丙三种不含结晶水的固体物质的溶解度曲线. 
①t1℃,若将4.0g甲物质放入10g水中充分溶解得到g溶液.
②将t2℃时甲、乙、丙三种物质的饱和溶液分别降温到t1℃时,则甲、乙、丙三种溶液溶质质量分数由大到小的顺序是 .
③t1℃时,一小试管内盛有甲物质的饱和溶液,试管底部还存有少许固体甲,将小试管放入盛有水的烧杯中,然后将多量的NaOH固体加入烧杯的水中,小试管内的固体物质逐渐溶解,原因是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】按要求写出下列化学方程式。
(1)正常雨水pH约为5.6的原因是_________________。
(2)波尔多液不能用铁制容器盛放的原因是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.稀有气体化学性质不活泼,常用作保护气
B.铜丝具有导电性,常用作导线
C.金刚石的硬度很大,常用于切割大理石
D.氧气能支持燃烧,常用作燃料
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为实验室中常见的气体制备、净化、收集和性质实验的部分仪器. 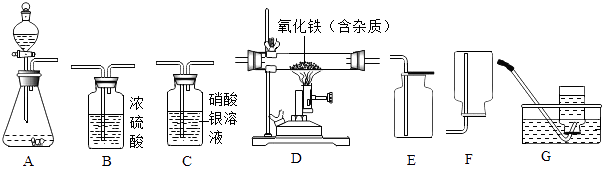
(1)若以石灰石和稀盐酸为原料制取二氧化碳气体,因盐酸会挥发出少量的氯化氢气体,导致制取的气体不纯,现要收集一瓶比较纯净干燥的二氧化碳气体. ①所选仪器的连接顺序为(填写仪器序号字母).
②生成二氧化碳时,所发生反应的化学方程式为 .
③实验室制取二氧化碳后的剩余废液中常含有少量盐酸,若在不用酸碱指示剂的条件下加入某种药品除去其中的盐酸,得到较纯净的中性液体,请从纯碱、熟石灰、石灰石三种物质中选用的一种试剂是 , 请简述实验过程 .
(2)若装置A中盛放锌粒和稀硫酸,小颖同学欲利用制备的氢气来测定10g氧化铁样品中氧化铁的纯度(杂质不反应),仪器连接顺序为:A→B1→D→B2→B3 . (已知:Fe2O3+3H2 ![]() 2Fe+3H2O,其中B1、B2、B3为3个浓硫酸洗气瓶) ①实验开始时,要先通一会儿H2再加热,理由是 .
2Fe+3H2O,其中B1、B2、B3为3个浓硫酸洗气瓶) ①实验开始时,要先通一会儿H2再加热,理由是 .
②若装置中不连接B1 , 用B2装置在反应前后质量的增加进行计算,则计算结果会 . (选填“偏大”、“偏小”、“不受影响”之一)
③若测得B2增加的质量为ag,则该样品中氧化铁的质量为 . (可为分数形式)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有X、Y、Z三种金属,为判断其活动性顺序,某兴趣小组的同学做了如下实验①将X、Y、Z分别置于稀硫酸中,X有气体产生,Y、Z无明显现象;②将Y金属放入Z的盐溶液中,Y表面有Z金属析出。则X、Y、Z的活动性顺序为( )
A.Y>Z>XB.X>Y>ZC.X>Z>YD.Y>X>Z
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氧气在日常生活和T业生产中的用途非常广泛,其实验室的制取是化学研究的重要内容。
(1)根据下列实验装置图回答问题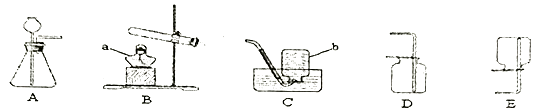
①写出标有字母的仪器名称:a ,b 。
②写出A装置制取O2的化学方程式 。
③若装置D收集氧气,验满的方法是 。
(2)实验室常用加热氯酸钾与二氧化锰混合物的方法制取氧气,写出反应的化学方程式: ;
(3)小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
【提出猜想】除MnO2 , CuO外,Fe2O3 , 也可以作KClO3分解的催化剂。
【实验验证】按下表进行实验:经测定分解温度(分解温度越低,催化效果越好)。
实验编号 | 实验药品 | 分解温度( |
① | KClO3 | 580 |
② | KClO3、MnO2质量比1:1) | 350 |
③ | KClO3 , CuO(质量比1:1) | 370 |
④ | KClO3、Fe2O3(质量比1:1) | 390 |
【分析数据、得出结论】由实验与实验④对比,证明猜想合理。
(4)【拓展延伸】如果将KMnO4固体与KClO3固体混合加热,则KClO3的分解速率大大加快。请说明KMnO4在KClO3的分解反应中是否作催化剂,为什么?
(5)【实验反思】同种催化剂,颗粒大小可能影响催化效果,请设计实验方案进行验证 。
(6)在实验室中用高锰酸钾制取氧气,若产生9.6克氧气需要分解克高锰酸钾?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某两种物质在一定条件下发生化学反应的微观示意图如图所示(其中“ ![]() ”和“
”和“ ![]() ”分别表示两种不同的原子).对上述反应,下列说法正确的是( )
”分别表示两种不同的原子).对上述反应,下列说法正确的是( ) 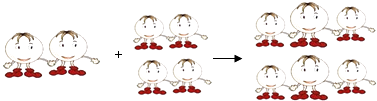
A.反应物都是化合物
B.反应属于分解反应
C.生成物可能是氧化物
D.反应前后分子种类不变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据甲乙物质的溶解度曲线回答下列问题: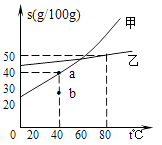
① 40℃时甲物质的溶解度是; 80℃时,乙物质在10g水中最多可以溶解g, 此时溶质的质量分数是。(精确到0.1%)
②甲中混有少量的乙,提纯甲物质的方法是。
③将b点的甲溶液转化为a点的甲溶液,采取的方法是(选填编号)。
A.增加溶质 B.恒温蒸发溶剂 C.升高温度 D.降低温度
④将80℃时甲乙的饱和溶液分别降温到20℃,下列说法正确的是。
A.析出固体的质量:甲>乙 B.降温后溶质的质量分数:甲<乙
C.降温后溶剂质量:甲<乙 D.降温后溶质质量:甲<乙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com