
有一矿山上的石灰石样品中只含杂质二氧化硅(二氧化硅是一种既不溶于水,也不与盐酸反应的固体)。小琳和她的同学想测定该样品中碳酸钙的质量分数。他们取一块石灰石样品,将其粉碎后,称出9.4g放入烧杯内(烧杯的质量为60.8g),然后慢慢加入稀盐酸,用玻璃棒搅拌至不再产生气泡为止,共用去稀盐酸97.8g。再称出反应后烧杯及其内物质的总质量为164.7g。试回答:
(1)将石灰石样品粉碎的主要目的是 。
(2)实验结束后,共放出二氧化碳 g(假设溶解在水中的二氧化碳质量忽略不计)。
(3)该石灰石样品中碳酸钙的质量分数是多少?(计算结果精确到0.1%)
(4)反应后溶液的质量为 g。
(1)为了增大反应物的接触面积,使反应能快速进行
(2)3.3g
(3)79.8%
(4)102
解析试题分析:(1)为避免样品中碳酸钙不能完成反应,可把样品粉碎,增大样品与盐酸的接触面积,此举还可以加快反应的速率;
(2)根据质量守恒定律可以知道放出气体二氧化碳的质量=9.4g+60.8g+97.8g-164.7g=3.3g
(3)设石灰石样品中碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 2.2g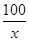 =
= 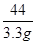
解得:x=7.5g
该石灰石中w(CaCO3)= 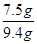 ×100%=79.8%
×100%=79.8%
答:该石灰石样品中碳酸钙的质量分数是79.8%.
(4)反应后溶液的质量为:164.7g-60.8g-(9.4g-7.5g)=102g
考点:根据化学反应方程式的计算


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:计算题
将117.0g氯化钠溶液与140.0g的硝酸银溶液混合,恰好完全反应,过滤后所得溶液的质量为228.3g。计算该氯化钠溶液的溶质质量分数?
(反应的化学方程式为NaCl+AgNO3=AgCl↓+NaNO3)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
张南同学为测定某赤铁矿样品中氧化铁的含量,取10g此样品,分五次向其中加入稀硫酸使之充分反应(假设样品中杂质不与稀硫酸反应,也不溶于水)。每次加入的稀硫酸质量及测定剩余固体的质量,记录数据如下表:
| | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
| 加入稀硫酸的质量/g | l0 | l0 | l0 | l0 | l0 |
| 剩余固体质量/g | 8.4 | 6.8 | 5.2 | 3.6 | 3.6 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
造纸是我国古代四大发明之一,它有效地推动了人类文明的发展。
(1)回收农田产生的秸秆作为造纸原料,可以减少焚烧秸秆带来的 污染。秸秆的主要成分是纤维素[(C6H10O5)n],纤维素中C、H、O三种元素的质量比为 (用最简整数比表示)。
(2)造纸会产生大量含NaOH的碱性废水,需经处理呈中性后排放。
①检测废水呈碱性的简单方法是 。
②若某造纸厂废水中NaOH的质量分数为1.6%,现有废硫酸9.8 t(H2SO4的质量分数为20%),可以处理的废水质量是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某石灰厂需要测定产品生石灰中杂质(杂质只含CaCO3)的质量分数。小刚进行了如图实验。请计算:
(1)生成CO2气体的质量;
(2)样品中CaCO3的质量分数。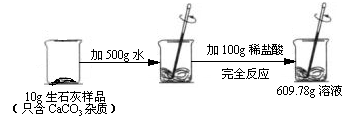
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
发射通信卫星的火箭用化学反应2N2H4+N2O4 3X+4H2O为动力来源.
3X+4H2O为动力来源.
(1)上述化学反应中X的化学式是 _________ ;
(2)请计算320g N2H4完全燃烧时消耗N2O4的质量.
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
有一研究性学习小组为测定某铜锌合金的成分,取10g该合金经粉碎后放入烧杯中,再加入足量的稀硫酸,反应过程中烧杯内固体物质的质量与反应时间的关系如下图所示。请回答下列问题。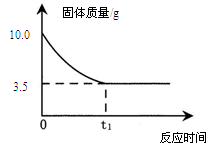
(1)将合金粉碎的目的是 。
(2)10g合金中铜的质量为 g。
(3)充分反应后产生的氢气质量为多少?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
碳和碳的氧化物是生活中常见的物质,也是初中化学学习的重要内容.
(1)如图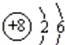 是,下列说法不正确的是 .
是,下列说法不正确的是 .
| A.氧原子的质子数为8 |
| B.氧原子在化学反应中易失去电子 |
| C.氧是地壳中含量最多的元素 |
| D.氧原子与氧离子的化学性质不同 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某工厂欲用2%的稀硫酸测定本厂排放的废水中氢氧化钾的含量(废水中的其他物质不与稀硫酸反应)。试计算:向盛有20 g废水的锥形瓶中逐滴滴加2%的稀硫酸,至恰好完全反应。将实验所得数据绘制成如图所示图像。求废水中氢氧化钾的质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com