
分析 探究一:根据CaCl2和MgCl2,与NaOH和Na2CO3反应的情况进行判断;
探究二:根据碳酸钠与氯化钙反应的情况解答.
(1)根据粗盐提纯的过程解答:根据氢氧化钠能和氯化镁反应生成白色沉淀氢氧化镁和氯化钠;Na2CO3与CaCl2反应生成白色沉淀碳酸钙和氯化钠;
(2)根据碳酸钠和氯化钙反应生成白色沉淀碳酸钙和氯化钠进行解答;
(3)根据碳酸钙的质量可以计算氯化钙的质量,从而可以计算氯化钠的质量,进一步可以计算这包粗盐含有NaCl的质量分数.
解答 解:
探究一:
①因为氯化镁与氢氧化钠反应生成氢氧化镁沉淀,而氯化钙与氢氧化钠反应没有沉淀或气体生成,加入数滴NaOH溶液,目的是检验有没有氯化镁;
②因为Na2CO3溶液与CaCl2反应生成碳酸钙沉淀,故加入数滴Na2CO3溶液,目的是检验其有没有氯化钙;
故答案为:MgCl2,CaCl2;
探究二:
②③⑤步骤中,都使用到同一仪器为玻璃棒.②中玻璃棒的作用是加速粗盐的溶解;③中玻璃棒的作用是;⑤中玻璃棒的作用是防止由于局部温度过高,造成液滴飞溅;步骤③中加入试剂是Na2CO3,碳酸钠与氯化钙反应的化学方程式为CaCl2+Na2CO3=CaCO3↓+2NaCl;步骤⑤进行的“某一操作”是加入适量或过量的稀盐酸,目的是除去过量的碳酸钠,反应的化学方程式为:Na2CO3+2HCl=2NaCl﹢H2O﹢CO2↑;步骤⑥中需要称量的固体是A,因为B中含有反应生成的氯化钠.
故答案为:
(1)MgCl2;CaCl2;
(2)Na2CO3;加入适量或过量的稀盐酸;
(3)A,B中含有反应生成的氯化钠.
点评 本题主要考查学生对粗盐提纯的实验的掌握.探究二中步骤④沉淀洗涤后小心烘干,得到纯净固体A是碳酸钙,步骤⑥称量实验中得到的固体A(碳酸钙)的质量,根据化学方程式可计算出CaCl2的质量,根据题意可知这包粗盐含有的杂质是 CaCl2,则这包粗盐中氯化钠的质量分数=$\frac{粗盐的质量-氯化钙的质量}{粗盐的质量}$×100%.


科目:初中化学 来源: 题型:选择题
| 编号 | 实验事实 | 实验结论 |
| A | 某溶液使酚酞溶液变红 | 该溶液一定是NaOH溶液 |
| B | 某物质中含有一种元素 | 该物质一定是单质 |
| C | 常温下,测定某溶液的PH=3 | 该溶液一定呈酸性 |
| D | 某气体不能使带火星的木条复燃 | 该气体一定不含氧气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 时间 (min) 浓度 条件 | 30%H2O2 | 15%H2O2 | 5%H2O2 |
| 加入agMnO2 | 0.2 | 0.8 | 2.0 |
| 加入agFe2O3 | 7.0 | 9.0 | 16.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
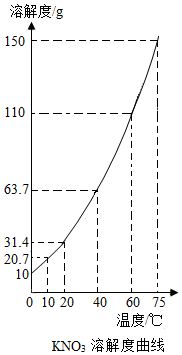 某固态混合物中含有mgKNO3和若干不溶于水的杂质,将它加入ng水中,在10℃、40℃、75℃时观察,充分溶解后的结果如表:
某固态混合物中含有mgKNO3和若干不溶于水的杂质,将它加入ng水中,在10℃、40℃、75℃时观察,充分溶解后的结果如表:| 温度 | 10℃ | 40℃ | 75℃ |
| 未溶固体 | 261g | 175g | 82g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com