
 为测定某氮肥中硫酸铵的纯度(即质量分数)是否与如图标签相符,小林取一定量该氮肥样品与烧杯中配成溶液与足量氯化钡溶液反应,记录有关数据如表
为测定某氮肥中硫酸铵的纯度(即质量分数)是否与如图标签相符,小林取一定量该氮肥样品与烧杯中配成溶液与足量氯化钡溶液反应,记录有关数据如表| 反应前 | 反应后 | |
| 烧杯和样品溶液总质量 | 氯化钡溶液质量 | 过滤后烧杯和溶液总质量(滤液的损失忽略不计) |
| 45g | 55g | 76.7g |
分析 根据质量守恒定律可知,过程中质量的减少是因为生成了硫酸钡,所以可以求算硫酸钡的质量,根据硫酸钡和对应的化学方程式求算硫酸铵的质量,进而求算对应的质量分数.
解答 解:
根据质量守恒定律可得,生成的硫酸钡的质量为45g+45g-76.7g=23.3g
设硫酸铵的质量为x
(NH4)2SO4+BaCl2═BaSO4↓+2NH4Cl
132 233
x 23.3g
$\frac{132}{233}$=$\frac{x}{23.3g}$
x=13.2g
氮肥中硫酸铵的纯度:$\frac{13.2g}{15g}$×100%=88%<96%,故不符合标准;
反应过程中,硫酸铵和氯化钡反应,导致硫酸根和钡离子结合生成难溶性硫酸钡沉淀,溶液中硫元素转化为硫酸钡的形式沉淀,所以溶液中硫元素的质量减少.
故填:
(1)23.3.
(2)符合;
(3)减小;反应后,硫酸根转化到硫酸钡中沉淀下来,故溶液中硫元素的质量减小.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | 用甲醛溶液浸泡海产品保鲜 | |
| B. | 若误服重金属盐,可立即饮用大量的牛奶,并马上送医院诊治 | |
| C. | 微量元素是人体必需的营养素,多吃无害 | |
| D. | 有机物都是含碳的化合物,CO、CO2也是有机物 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
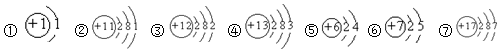
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
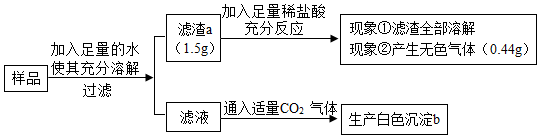
| A. | 滤渣a是CaCO3 | |
| B. | 白色沉淀b中可能含有MgCO3 | |
| C. | 滤液中一定存在的溶质是NaCl、BaCl2、NaOH | |
| D. | 该白色固体样品中一定含有CaCO3、BaCl2、NaOH、MgCl2,可能含有Na2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
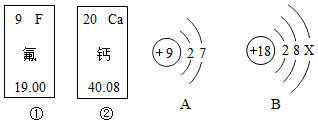
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
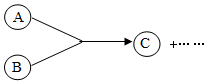 一定条件下,A和B物质转化为C物质的关系如图所示(部分条件和部分物质未标出)
一定条件下,A和B物质转化为C物质的关系如图所示(部分条件和部分物质未标出)查看答案和解析>>
科目:初中化学 来源: 题型:解答题
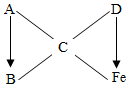 现有铁、氧化铁、稀盐酸、氢氧化钠、碳酸钠等五种物质,它们之间存在如图所示相互反应和转化关系(“-”表示相连的物质间能反应,“→”表示物质间的转化).回答下列问题
现有铁、氧化铁、稀盐酸、氢氧化钠、碳酸钠等五种物质,它们之间存在如图所示相互反应和转化关系(“-”表示相连的物质间能反应,“→”表示物质间的转化).回答下列问题查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com