
【题目】老师要求用规定的BaCl2溶液与适量的Na2SO4溶液制备BaSO4。完成操作Ⅰ后,小红发现自己错把Na2CO3溶液当成Na2SO4溶液,而此时BaCl2溶液已完全消耗。老师启发他,可用生成物和其他试剂完成制备BaSO4的实验。整个实验流程如图所示:

(1)试剂M是__________,气体C是__________。
(2)操作Ⅱ的名称是_________。
(3)反应①的化学方程式为________,溶液a中溶质是_______。
(4)反应③的基本反应类型为___________。
(5)从理论上讲,该实验过程最终得到的BaSO4质量与原方案得到的BaSO4质量是否相等?_________(填“是”或“否”)。
【答案】盐酸 CO2 蒸发结晶 BaCl2+ Na2CO3=2NaCl+BaCO3↓ NaCl 复分解反应 是
【解析】
反应①BaCl2 + Na2CO3= BaCO3↓+2NaCl固体B为BaCO3, 溶液a为NaCl溶液,由最后的反应物为BaSO4,可推测需要先加酸溶解BaCO3,滤液再和Na2SO4生成BaSO4沉淀,因此M试剂为盐酸,N为Na2SO4,选用HCl溶解BaCO3, 会生成CO2气体,故C为CO2,因为HCl过量,因此溶液b中溶质含有BaCl2和HC1;
(1)分析得:M为盐酸气体C是二氧化碳,故填:盐酸;CO2。
(2)氯化钠溶液蒸发结晶得到氯化钠,故填:蒸发结晶。
(3)由分析可得反应①化学方程式为BaCl2 + Na2CO3= BaCO3↓+2NaCl,固体B为BaCO3, 溶液a为NaCl溶液,故填:BaCl2 + Na2CO3= BaCO3↓+2NaCl;NaCl。
(4)反应③硫酸钠和氯化钡反应生成氯化钠和硫酸钡沉淀,两种化合物交换成分生成另外两种化合物,属于复分解反应,故填:复分解反应。
(5)根据质量守恒定律,BaCl2转化为 BaSO4中Ba原子守恒,可以判断实验过程最终得到的BaSO4质量与原方案得到的BaSO4质量相等,故填:是。


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:初中化学 来源: 题型:
【题目】某化学活动小组在一次实验中进行如下所示实验:
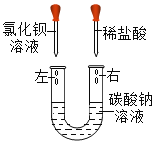
此时观察到U型管右侧产生的现象是___________________________,实验后,小组同学充分振荡U型管,发现管内仍有白色固体残留,将混合物过滤后,同学们对滤液成分产生了浓厚的兴趣,于是进行了进一步的探究活动。
(提出问题):滤液中可能含有哪些物质?
(猜想与假设):猜想一:溶质为NaCl
猜想二:溶质为NaCl和BaCl2
猜想三:溶质为______
(实验探究):小红为验证滤液的成分,取滤液于试管中,向其中滴加少量的硫酸钠溶液,观察到无明显现象。由此得出结论:猜想一成立。小刚认为小红的结论不严密,因为____________________________。
为验证三的猜想请填写下表:
实验过程 | 实验现象 | 实验结论 |
取少量滤液滴加_____ | 溶液变红 | 猜想三正确 |
(归纳与总结):通过上述实验我们能够总结出:在确定化学反应前后所得溶液中溶质成分时除了考虑生成物外,还要考虑__________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是盐酸性质的知识归纳,下列表达不正确的是( )
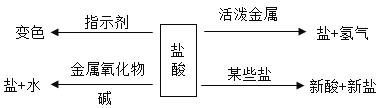
A.若盐为AgNO3溶液,则反应中有白色沉淀生成
B.若碱为NaOH的溶液,可以在溶液中滴加酚酞溶液,证明两者发生了中和反应
C.若金属氧化物为铁锈的主要成分,可以利用盐酸与金属氧化物反应的这一性质,除去铁锈
D.若金属为Mg和Zn,将过量的两种金属分别与等质量等浓度的一定量的稀盐酸完全反应,Mg产生的H2多
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请从A或B两题中任选一个作答,若两题均作答,按A计分。
A | B |
(1)电解水实验揭示了水的组成。下图实验中得到氧气的试管是_______(填“1”或“2”)。 (2)电解水的化学方程式为_________。
| (1)潜水时需要氧气,说明氧气能________。 (2)用高锰酸钾制取氧气的化学方程式为_________。
|
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一定条件下,下列物质在密闭容器内充分反应,测得反应前后各物质的质量如下:
纯净物 | 乙醇 | 氧气 | 二氧化碳 | 水 | X |
反应前质量/g | 2.3 | 4 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 2.2 | 2.7 | 待测 |
A.反应后X的质量为1.5g B.X中一定含有碳元素和氧元素
C.X中一定含有碳元素和氢元素 D.X中两种元素的质量比是1:1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列实验装置图,回答相关问题。
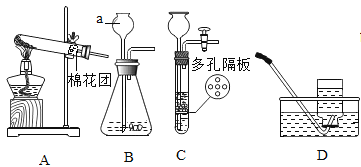
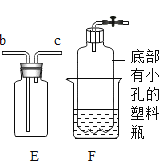
(1)图中标有 a 的仪器名称是____
(2)用高锰酸钾制取较纯净的氧气,装置组合是__(填字母),化学方程式为____,试管口放一团棉花的作用是__。
(3)实验室制取二氧化碳的化学方程式为___,
选择 E 装置收集二氧化碳,气体应从___(填“b”或“c”)端通入。小明组装了 F 装置用于制取二氧化碳,该装置能达到的效果相当于图中的__(填字母)装置,F 装置中的石灰石可用_________(填字母)替代。
A 大理石
B 洗净的鸡蛋壳
C 苏打粉
(4)在20mL溶质质量分数为1.60%的硫酸铜溶液中,逐滴加入某浓度的氢氧化钡溶液,用电导仪测得溶液的电导率(电导率越高表示溶液的导电性越好),如图所示。溶液的pH随滴入Ba(OH)2溶液体积的变化曲线(假设所有稀溶液的密度均为l g/cm3),如图所示:
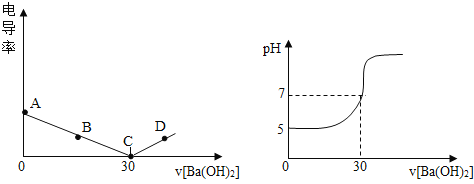
①硫酸铜和氢氧化钡溶液发生反应的化学方程式为:_________。
②图中C点所示溶液中,含量较多的微粒是水分子,D点所示溶液能导电是因为溶液中含有_______(填粒子符号)。
③由图可知:将打磨过的铝片放入上述硫酸铜溶液中,可以观察到的现象是:铝片表面有红色物质生成,溶液由蓝色逐渐变无色,同时还可以看到 ___。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室通常用澄清石灰水检验二氧化碳的存在,若二氧化碳过量,会进一步与碳酸 钙、水反应生成易溶于水的碳酸氢钙(CaCO3+H2O+CO2═Ca(HCO3)2)。若向含有 Ca(OH)2 7.4g 的澄清石灰水里缓缓通入一定量的二氧化碳,反应后若生成 5g 沉淀,则通 入二氧化碳的质量可能为( )
A.2.2gB.4.4gC.6.6gD.13.2g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳酸乙烯酯(C3H4O3)可用作锂电池电解液,下列有关碳酸乙烯酯的说法正确的是
A. 碳酸乙烯酯的相对分子质量为(12×3+1×4+16×3)g
B. 碳酸乙烯酯中C、H、O三种元素的质量比为12:1:16
C. 碳酸乙烯酯中C、H、O三种原子的个数比为3:4:3
D. 碳酸乙烯酯中碳元素的质量分数= ![]() ×100%
×100%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】a、b、c 三种物质的溶解度曲线如下图所示。取等质量![]() ℃的 a、b、c 三种物质的饱和溶液,分别蒸发等量水后恢复至
℃的 a、b、c 三种物质的饱和溶液,分别蒸发等量水后恢复至![]() ℃。下列说法不正确的是
℃。下列说法不正确的是
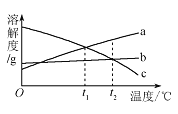
A. 原饱和溶液中,溶质的质量分数 a>b="c"
B. 恢复至 t2℃时,析出溶质的质量 a>b=c
C. 恢复至t2℃时,三种溶液一定都是饱和溶液
D. 若继续降温至 t1℃,三种溶液一定都是饱和溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com