
���� ��1����������������������ش�
��2������п����λ�����ǰ�ߣ�����ϡ���ᷴӦ�����ش�
��3���ڽ������˳���У���ǰ�Ľ��������ᷴӦ����������λ����ǰ�Ľ����ܽ�λ�����Ľ�����������Һ���û��������ݴ˷����жϣ�
��� �⣺��1���������Ҫ�ɷ֣�Fe2O3?xH2O���������������������ˮ��������ͬ���ã�
��2�������ֽ����ֱ����ϡ�����У�п����λ�����ǰ�ߣ�����ϡ���ᷴӦ��������Ӧ�Ļ�ѧ����ʽ�ǣ�Zn+H2SO4=ZnSO4+H2����Fe+H2SO4=FeSO4+H2����
��3�����ڽ����Ļ����Zn��Cu��Ag����AgNO3��Cu��NO3��2�Ļ����Һ�м���һ������Zn�ۣ�п������������Ӧ������������Ӧ��ȫ����������ͭ��Ӧ����ַ�Ӧ���ˣ���ҺΪ��ɫ����Һ��һ�����е�������Cu��NO3��2��Zn��NO3��2��
�ʴ�Ϊ����1������ˮ��������ͬ���ã�
��2��Zn+H2SO4=ZnSO4+H2����Fe+H2SO4=FeSO4+H2��
��3��Cu��NO3��2��Zn��NO3��2��
���� ������Ҫ�����˽������˳���Ӧ�ã���ɴ��⣬�������ݽ������˳����������У�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
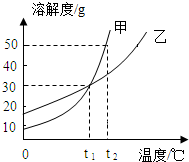 ��ͼΪ�ס����������ʵ��ܽ�����ߣ���ش��������⣺
��ͼΪ�ס����������ʵ��ܽ�����ߣ���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������̼��������ɵ� | B�� | ����������л��� | ||
| C�� | ������̼����Ԫ�ص�������Ϊ3��1 | D�� | ����ȼ������ˮ�Ͷ�����̼ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
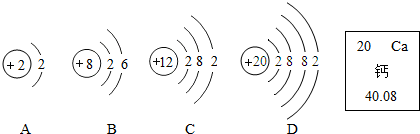
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaCl | B�� | Ca��OH��2 | C�� | H2O | D�� | O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
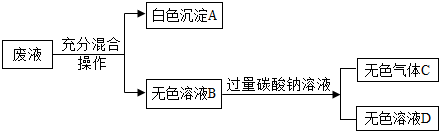
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
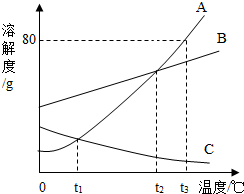 ��ͼ��A��B��C�������ʵ��ܽ�����¶ȱ仯������ͼ������ͼ�ش�
��ͼ��A��B��C�������ʵ��ܽ�����¶ȱ仯������ͼ������ͼ�ش��鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com