
”¾ĢāÄæ”æŹµŃéŹŅ³£ÓĆĻĀĶ¼ĖłŹ¾µÄ×°ÖĆÖĘČ”ĘųĢåŗĶĘųĢåŠŌÖŹµÄŃéÖ¤£¬Ēė»Ų“š£ŗ
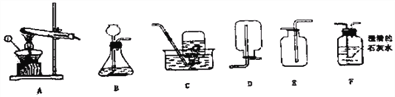
(1)ŅĒĘ÷¢ŁµÄĆū³Ę___________”£
(2)ŹµŃéŹŅÓĆøßĆĢĖį¼ŲÖĘČ”ŃõĘų£¬æÉєȔµÄŹÕ¼Æ×°ÖĆŹĒ_______(ĢīŠņŗÅ)£¬·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ__________________________________”£
(3)ijĶ¬Ń§ĄūÓĆŹÆ»ŅŹÆŗĶŃĪĖįĶعż×°ÖĆB”¢FĄ“ŃéÖ¤¶žŃõ»ÆĢ¼µÄŠŌÖŹ£¬ŹµŃé¹ż³ĢÖŠ¹Ū²ģµ½FÖŠÓŠĘųÅŻĆ°³ö£¬³ĪĒåµÄŹÆ»ŅĖ®Ī“±ä»ė×Ē£¬ŹŌ·ÖĪöĘäæÉÄܵÄŌŅņ______”£
”¾“š°ø”æ ¾Ę¾«µĘ C»ņE 2KMnO4![]() K2MnO4+MnO2+O2”ü ŃĪĖįÅØ¶Č¹ż“ó
K2MnO4+MnO2+O2”ü ŃĪĖįÅØ¶Č¹ż“ó
”¾½āĪö”æ(1)¾ŻĶ¼æÉÖŖŅĒĘ÷¢ŁŹĒ¾Ę¾«µĘ£»(2)ŹµŃéŹŅÓĆøßĆĢĖį¼ŲÖĘČ”ŃõĘų£¬ŃõĘųµÄĆܶȓóÓŚæÕĘųµÄĆÜ¶Č£¬¶ųĒŅ²»Ņ×ČÜÓŚĖ®£¬ĖłŅŌæÉŅŌÓĆC»ņE×÷ĪŖŹÕ¼Æ×°ÖĆ£»·“Ó¦µÄ·½³ĢŹ½ŹĒ2KMnO4![]() K2MnO4+MnO2+O2”ü£»(3)Čō¶žŃõ»ÆĢ¼ĘųĢå²»ÄÜŹ¹ŹÆ»ŅĖ®±ä»ė×Ē£¬æÉÄÜŹĒŃĪĖįÅØ¶Č¹ż“ó»Ó·¢³öĀČ»ÆĒāĘųĢ壬ÓėĒāŃõ»ÆøĘ·¢ÉśĮĖ·“Ó¦”£
K2MnO4+MnO2+O2”ü£»(3)Čō¶žŃõ»ÆĢ¼ĘųĢå²»ÄÜŹ¹ŹÆ»ŅĖ®±ä»ė×Ē£¬æÉÄÜŹĒŃĪĖįÅØ¶Č¹ż“ó»Ó·¢³öĀČ»ÆĒāĘųĢ壬ÓėĒāŃõ»ÆøĘ·¢ÉśĮĖ·“Ó¦”£


 ŠĀĖ¼Ī¬ŗ®¼Ł×÷ŅµĻµĮŠ“š°ø
ŠĀĖ¼Ī¬ŗ®¼Ł×÷ŅµĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĀČ»ÆŃĒĶ(CuCl)¹ć·ŗÓ¦ÓĆÓŚŅ±½š”¢µē¶Ę”¢Ņ½Ņ©µČŠŠŅµ”£ŅŃÖŖCuClÄŃČÜÓŚĖ®ŗĶŅŅ“¼£¬ŌŚ³±ŹŖæÕĘųÖŠŅ×±äÖŹ”£CuClµÄÖʱøĮ÷³ĢČēĻĀ£ŗ
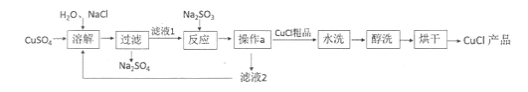
£Ø1£©”°ĀĖŅŗ1”±ÖŠ³żĮĖNa+”¢SO42-Ķā£¬»¹“ęŌŚ½Ļ¶ąµÄĄė×ÓŹĒ ”¢ £ØŠ“Ąė×Ó·ūŗÅ£©
£Ø2£©”°·“Ó¦”±ÖŠ·¢ÉśµÄ»Æѧ±ä»ÆŹĒ2CuCl2+Na2SO3=2CuCl”ż+2NaCl+SO3£¬²śÉśµÄSO3ŃøĖŁÓėĖ®»ÆŗĻÉś³ÉŅ»ÖÖĖį£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ ”£
£Ø3£©”°²Ł×÷a”±µÄĆū³ĘŹĒ ”£±¾Į÷³ĢÖŠæÉŅŌŃ»·ĄūÓƵÄĪļÖŹ£ØĖ®³żĶā£©ŹĒ ”££ØŠ“»ÆѧŹ½£©
£Ø4£©æÉÓĆ”°Ė®Ļ“”±µÄŌŅņŹĒ £¬”°“¼Ļ“”±µÄÄæµÄŹĒ ”£
£Ø5£©160g CuSO4Óė×ćĮæNaCl¾ÉĻŹöÖʱøĮ÷³Ģ£¬æÉÉś³ÉµÄCuCl×ī¶ąŹĒ g”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĀČ»ÆøĘŌŚÉś»īÖŠ³£ÓĆ×÷øÉŌļ¼Į”¢ČŚŃ©¼Į£¬ŌŚ¹¤ŅµÉĻæÉÓĆÓŚÖĘŌģ·Ą¶³ŅŗµČ”£Ä³¹¤³§ŅŌŹÆ»ŅŹÆĪŖŌĮĻÉś²śĀČ»ÆøĘ¾§ĢåµÄĮ÷³ĢČēĻĀ”£ŌĮĻŹÆ»ŅŹÆÖŠŗ¬ÓŠŌÓÖŹÖ÷ŅŖŹĒMgCO3”¢MgSO4 ŗĶAl2O3”£
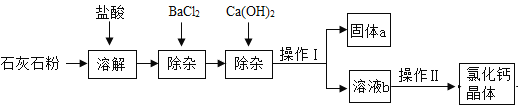
¢ÅŹÆ»ŅŹÆ·ŪČܽāŹ±£¬Al2O3·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ________________”£
¢Ę¼ÓČėBaCl2³żČ„µÄŌÓÖŹĄė×ÓŹĒ____________(ĢīĄė×Ó·ūŗÅ)£»
¢Ē²Ł×÷¢ńµÄĆū³ĘĪŖ____________£¬ŠčÓƵ½µÄŹµŃéŅĒĘ÷ÓŠ£ŗĢś¼ÜĢØ(“ųĢśČ¦)”¢Ā©¶·”¢ÉÕ±”¢____________”£²Ł×÷¢ņµÄ¾ßĢå²½ÖčĪŖ£ŗ____________”¢ĄäČ“½į¾§”£
¢Č¹ĢĢåaµÄ³É·ÖŅ»¶Øŗ¬ÓŠ________________________(Ö»Š“Ņ»ÖÖ)”£¼ģŃéČÜŅŗbµÄĖį¼īŠŌ£¬Čē¹ūĻŌ¼īŠŌ£¬»¹Šč¼ÓČėŹŹĮæµÄ____________ (Ģī»ÆѧŹ½)Ģįøß²śĘ·“æ¶Č”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪ¢¹ŪŹ¾ŅāĶ¼æÉŅŌŠĪĻóµÄ±ķŹ¾ĪļÖŹ·¢ÉśµÄĪ¢¹Ū±ä»Æ
(1)ĒėŌŚĻĀĶ¼µŚŅ»”¢Čż·½æņÖŠ°ŃĮņ»ÆĒāŌŚŃõĘųÖŠČ¼ÉÕ(2H2S+3O2![]() 2SO2+2H2O)µÄĪ¢¹ŪŹ¾ŅāĶ¼²¹»ĶźÕū”£______________
2SO2+2H2O)µÄĪ¢¹ŪŹ¾ŅāĶ¼²¹»ĶźÕū”£______________
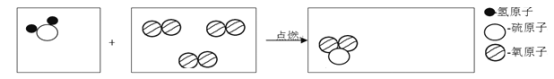
(2)ŌŚÉĻŹö»Æѧ·“Ó¦ÖŠ£¬»ÆŗĻ¼Ū²»·¢ÉśøıäµÄŌŖĖŲŹĒ_________(Ģī·ūŗÅ)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŖ²ā¶ØĶŠæŗĻ½šÖŠŠæµÄÖŹĮæ·ÖŹż£¬½ųŠŠĮĖŅŌĻĀŹµŃé£»Č”40gĶŠæŗĻ½š·ÅČėÉÕ±ÖŠ£¬³ĘµĆÉÕ±¼°ĖłŹ¢ĶŠæŗĻ½šµÄ×ÜÖŹĮæĪŖ140g£¬ŌŁ°Ń120gŃĪĖįĘ½¾ł·Ö³ÉĖÄ·ŻŅĄ“Ī¼ÓČėÉÕ±ÖŠ£¬Ćæ“Ī³ä·Ö·“Ó¦ŗó½ųŠŠ³ĘĮ棬ŹµŃ鏿¾ŻČēĻĀ£ŗ
Ėł¼ÓŃĪĖįµÄ“ĪŹż | µŚŅ»“Ī | µŚ¶ž“Ī | µŚČż“Ī | µŚĖÄ“Ī |
ÉÕ±¼°ĖłŹ¢ĪļÖŹµÄ×ÜÖŹĮæ/g | 169.7 | 199.4 | 229.2 | 259.2 |
ĒėÄć¾Ż“Ė·ÖĪö¼ĘĖć£ŗ
(1)µŚŅ»“ĪŹµŃéÉś³ÉĒāĘųµÄÖŹĮæŹĒ ________ g£®
(2)ĄūÓƵŚŅ»“ĪŹµŃéµÄŹż¾Ż£¬¼ĘĖć30gŃĪĖįÖŠČÜÖŹµÄÖŹĮæ·ÖŹż________ (Š“³ö¼ĘĖć¹ż³Ģ£¬¾«Č·µ½0.1%)
(3)ŹµŃé×īÖÕ½įŹųŗó£¬Ķ¬Ń§ĆĒĒó³öĮĖŗĻ½šÖŠŠæµÄÖŹĮæ·ÖŹż=__________.
(4)ĻĀĶ¼±ķŹ¾Ėł¼ÓŃĪĖįµÄÖŹĮæÓė·“Ó¦ŗóĖłµĆČÜŅŗÖŹĮæµÄ¹ŲĻµĒśĻߣ¬ĒėŠ“³öAµć(X=______ ,Y=______)µÄ×ų±ź”£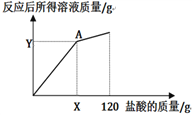
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĒėøł¾ŻĻĀĶ¼»Ų“šĪŹĢā£ŗ
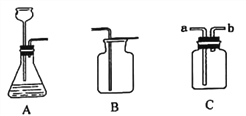
(1)ČōÓĆ×°ÖĆCŹÕ¼ÆŃõĘų£¬ĘųĢå“Ó___________(Ģī”°a”±»ņ”°b”±)¶ĖĶØČė”£
(2)ČōŃ”ÓĆ×°ÖĆA”¢BŗĶCÖĘČ”²¢ŹÕ¼ÆøÉŌļµÄ¶žŃõ»ÆĢ¼£¬ŌņŠč½«×°ÖĆAÖŠµÄ“ķĪóøÄÕżĪŖ________£¬×°ÖĆCÖŠÓ¦Ź¢·ÅµÄŅŗĢåŹŌ¼ĮĪŖ_________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĄūÓĆĻĀĮŠø÷×éĪļÖŹ²»ÄÜŃéÖ¤Fe”¢Cu”¢AgČżÖÖ½šŹō»ī¶ÆŠŌĖ³ŠņµÄŹĒ![]()
A. Cu”¢![]() ČÜŅŗ”¢
ČÜŅŗ”¢![]() ČÜŅŗ B. Fe”¢Cu”¢Ag”¢Ļ”ŃĪĖį
ČÜŅŗ B. Fe”¢Cu”¢Ag”¢Ļ”ŃĪĖį
C. Fe”¢Ag”¢![]() ČÜŅŗ D. Fe”¢Cu”¢Ļ”ĮņĖį”¢
ČÜŅŗ D. Fe”¢Cu”¢Ļ”ĮņĖį”¢![]() ČÜŅŗ
ČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŅ¹ś»Æѧ¼ŅŗīµĀ°ń£ØČēĶ¼£©øÄøļ¹śĶāµÄ“æ¼īÉś²ś¹¤ŅÕ£¬Éś²śĮ÷³ĢæɼņŅŖ±ķŹ¾ČēĻĀ£ŗ


£Ø1£©ÉĻŹöÉś²ś“æ¼īµÄ·½·Ø³Ę____________________£¬ø±²śĘ·µÄŅ»ÖÖÓĆĶ¾ĪŖ_________________”£
£Ø2£©Ļņ³Įµķ³ŲÖŠĶØČėĮ½ÖÖĘųĢ壬ĻČĶØČėµÄŹĒ________________£ØĢī”°NH3”±»ņ”°CO2”±£©£¬³Įµķ³Ų·¢ÉśµÄ»Æѧ·“Ó¦·½³ĢŹ½ŹĒ_______________________________”£
£Ø3£©Š“³öÉĻŹöĮ÷³ĢÖŠXĪļÖŹµÄ»ÆѧŹ½_____________________”£
£Ø4£©Ź¹ŌĮĻĀČ»ÆÄʵĥūÓĆĀŹ“Ó70%Ģįøßµ½90%ŅŌÉĻ£¬Ö÷ŅŖŹĒÉč¼ĘĮĖ_____________£ØĢī”°Ń»·I”±»ņ”°Ń»·II”±£©”£“Ó³Įµķ³ŲÖŠČ”³öNaHCO3³ĮµķµÄ²Ł×÷ŹĒ__________________”£
£Ø5£©ĪŖ¼ģŃé²śĘ·Ģ¼ĖįÄĘÖŠŹĒ·ńŗ¬ÓŠĀČ»ÆÄĘ£¬æÉȔɣĮæŹŌŃłČÜÓŚĖ®ŗó£¬ĻȵĪ¼Ó×ćĮæµÄ_______£¬ÅųżNa2CO3µÄøÉČÅ£¬ŌŁµĪ¼Ó___________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¼×”¢ŅŅ”¢±ūČżÖÖ¹ĢĢåĪļÖŹµÄČܽā¶ČĒśĻßČēĻĀĶ¼ĖłŹ¾”£»Ų“š£ŗ
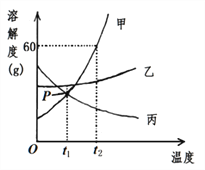
(1)Pµć±ķŹ¾µÄŅāŅåŹĒ£ŗ__________£»
(2)·Ö±š½«ČżÖÖĪļÖŹµÄ±„ŗĶČÜŅŗ“Ót2 ”ę½µÖĮt1 ”ę£¬ĖłµĆČÜŅŗÖŠČÜÖŹµÄÖŹĮæ·ÖŹżÓɓ󵽊”µÄĖ³ŠņŹĒ£ŗ____£»
(3)Óū“Óŗ¬ÉŁĮæŅŅµÄ¼×ÖŠ·ÖĄėĢį“æ¼×£¬Ó¦²ÉÓƵķ½·ØŹĒ£ŗ______£»
(4)t2 ”ꏱ£¬½«50 g¼×·ÅČė50 gĖ®ÖŠ£¬ĖłµĆČÜŅŗµÄÖŹĮæŹĒ__________g”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com