
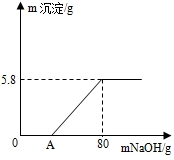
 向100g稀硫酸溶液中加入一定量的镁粉,待固体完全溶液后,再向所得溶液中加入质量分数为20%的NaOH溶液,所得沉淀的质量与加入NaOH溶液的质量关系如图所示,请回答下列问题:
向100g稀硫酸溶液中加入一定量的镁粉,待固体完全溶液后,再向所得溶液中加入质量分数为20%的NaOH溶液,所得沉淀的质量与加入NaOH溶液的质量关系如图所示,请回答下列问题:分析 (1)根据开始没有沉淀生成,说明硫酸过量,所以OA段是硫酸和NaOH溶液反应生成硫酸钠和水进行解答;
(2)根据生成沉淀氢氧化镁中镁元素的质量即为加入镁粉的质量进行解答;
(3)根据硫酸镁和氢氧化钠反应生成硫酸钠和氢氧化镁,硫酸和氢氧化钠反应生成硫酸钠和水,依据题中的数据减小计算.
解答 解:(1)开始没有沉淀生成,说明硫酸过量,所以OA段是硫酸和NaOH溶液反应生成硫酸钠和水,所以当加入NaOH溶液至A点时,烧杯内溶液中含有的溶质是硫酸镁、硫酸钠;
(2)生成沉淀氢氧化镁中镁元素的质量即为加入镁粉的质量,由图可知生成氢氧化镁的质量为5.8g,所以加入镁粉的质量=$\frac{24}{24+(16+1)×2}$×100%×5.8g=2.4g;
(3)根据题中的反应原理可知,镁和硫酸反应生成硫酸镁和氢气,硫酸镁和氢氧化钠会生成硫酸钠和氢氧化镁沉淀,硫酸和氢氧化钠会生成硫酸钠和水,所以可以运用氢氧化钠全部转化成硫酸钠进行计算,
反应后的溶液质量100g+2.4g+80g-0.2g=182.2g,
生成硫酸钠的质量为y,
2NaOH→Na2SO4
80 142
80g×20% y
$\frac{80}{80g×20%}$=$\frac{142}{x}$
y=28.4g,
所以溶质的质量分数为:$\frac{28.4g}{182.2g}$×100%=15.6%.
故答案为:(1)硫酸镁、硫酸钠;
(2)2.4;
(3)15.6%.
点评 本题主要考查学生利用化学方程式进行计算的能力.解题的关键是结合物质间反应的情况,正确分析图示数据,细心解答.


科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | SO2中的硫、氧元素的个数比为1:2 | B. | X的化学式是FeS2 | ||
| C. | 反应前后氧元素的化合价发生改变 | D. | Fe2O3中铁元素的质量分数为70% |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
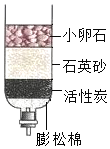 水与人类的生活和生产密切相关.
水与人类的生活和生产密切相关.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com