
| 实验步骤 | 实验现象 | |
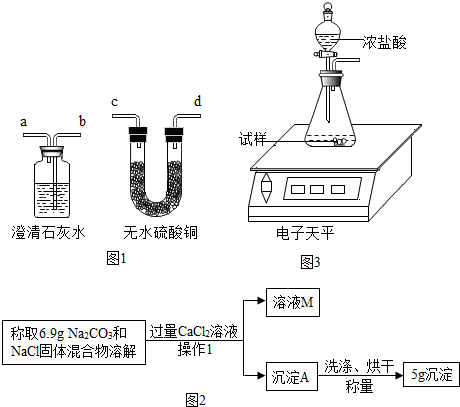
| 实验1 | 取样与试管中,加入食醋 并将产生气体通入澄清石灰水中. | 有气泡产生 石灰水变浑浊. |
| 实验2 | 取安多夫样品少许加入试管中,加热使之充分反应,并把产生的气体通入澄清石灰水. | 试管口出现小水珠,澄清石灰水变浑浊,试管中残留白色固体粉末. |
分析 【实验探究一】(2)根据题目信息和知识基础,确定检验CO2和水蒸气所用药品;
(2)①根据题意是将拌了安多夫粉的肉类放到锅中并加入食醋等调料烧煮,所以有两种情况:可能是自身分解生成二氧化碳;也可能是二者相互反应生成二氧化碳;
②根据碳酸氢钠的组成及碳酸钠和碳酸氢钠的稳定性和酸的反应进行分析解答.
【实验探究二】
(1)根据过滤可以将不溶性固体和液体分离解答;根据实验中加入过量CaCl2溶液的目的是使碳酸钠完全沉淀解答;
(2)根据确定沉淀A是否洗涤干净的方法是取最后一次洗涤液,证明是否含有氯离子或者钙离子等解答;
(3)根据沉淀的质量利用反应的关系式分析解答;
(4)根据题中的信息分析解答.
解答 解:
【实验探究一】
(1)根据题意,检验有无二氧化碳可用澄清的石灰水,检验水用无水硫酸铜,先检验水,在检验二氧化碳,故装置导气口连接顺序:气体样品→dcba
;
(2)①根据题意可知二氧化碳的生成可能有两种情况:碳酸氢钠自身分解生成二氧化碳;或者是碳酸氢钠与醋酸反应生成二氧化碳;
②实验1:取样与试管中,加入食醋,并将产生气体通入澄清石灰水中;有气泡产生并且石灰水变浑浊,猜想①正确;
实验2:取安多夫样品少许加入试管中,加热使之充分反应,并把产生的气体通入澄清石灰水.试管口出现小水珠,澄清石灰水变浑浊,试管中残留白色固体粉末.猜想②正确;
【实验探究二】
(1)操作1”的名称是过滤;实验中加入过量CaCl2溶液的目的是使碳酸钠完全沉淀;
(2)确定沉淀A是否洗涤干净的方法是取最后一次洗涤液,证明是否含有氯离子或者钙离子等;
(3)Na2CO3~CaCO3~2NaHCO3
106 100 168
x 5 g y
$\frac{106}{x}=\frac{100}{5g}=\frac{168}{y}$
x=5.3g
y=8.4g
样品中氯化钠的质量为6.9 g-5.3 g=1.6 g
样品中NaHCO3的质量分数=$\frac{8.4g}{8.4g+1.6g}×$100%=84%
(4)两位同学经过多次的实验测定后发现,得到的最终结果总是比真实值偏大,分析结果偏大的原因可能是实验中使用了浓盐酸,浓盐酸具有挥发性;未考虑反应过程中水的蒸发.
答案:
【实验探究一】
(1)dcba
(2)
①碳酸氢钠与醋酸反应生成的
②
| 实验步骤 | 实验现象 | |
| 实验1 | 取样与试管中,加入食醋 并将产生气体通入澄清石灰水中. | 有气泡产生 石灰水变浑浊. |
| 实验2 | 取安多夫样品少许加入试管中,加热使之充分反应,并把产生的气体通入澄清石灰水. | 试管口出现小水珠,澄清石灰水变浑浊,试管中残留白色固体粉末. |
点评 本题综合性强,主要通过实验考查了以下知识点:碳酸钠和碳酸氢钠的化学性质以及简单实验设计;平时要注意相关基础知识的记忆,方能熟练解答.


 优生乐园系列答案
优生乐园系列答案科目:初中化学 来源: 题型:解答题
 回答下列问题:
回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 乙二醇中氧元素的质量分数最大 | |
| B. | 乙二醇中C、H、O元素的质量比为12:3:16 | |
| C. | 乙二醇由2个碳原子、6个氢原子和2个氧原子构成 | |
| D. | 乙二醇相对分子质量为62 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 塑料、合金---合成材料 | B. | 洁净的空气、高锰酸钾---混合物 | ||
| C. | 豆浆、雪碧---溶液 | D. | 煤、天然气---化石燃料 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 葡萄糖由碳、氢、氧三种元素组成 | |
| B. | 葡萄糖的相对分子总质量为180 | |
| C. | 葡萄糖属于有机化合物 | |
| D. | 葡萄糖分子中含存6个碳原子和6个水分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com