
| 操作 | 现象 | 结论 | 装置 |
| 实验一: 同时将Ⅰ中5mL5%的过氧化氢溶液和Ⅱ中5mL15%的过氧化氢溶液注入各盛有0.5g二氧化锰的甲、乙中,关闭弹簧夹. | 发现烧杯中右侧导管口产生气泡的速率比左侧快. | 化学反应速率与 反应物浓度有关; 该反应的化学方程式为 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑. | 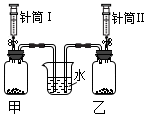 |
| 操作 | 现象 | 现象分析 | 装置 |
| 实验二: 先将稀盐酸注入甲,关闭弹簧夹;再将水注入乙,关闭弹簧夹. 注意:注入液体后,甲、乙导管口均处于液面以下. | 甲中液体先流入烧杯,乙中液体后流入烧杯,然后观察到烧杯中先无明显现象,后有白色沉淀产生. | 乙中液体流入烧杯的原因是 氢氧化钠溶于水,放出热量,使得瓶内压强大于外界压强; 甲中流入烧杯的液体溶质的化学式是 MgCl2HCl. | 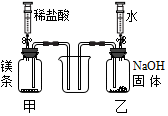 |
分析 根据实验方案设计要注意控制变量、物质间反应的现象以及化学方程式的书写的知识进行分析解答即可.
解答 解:要比较反应速率的影响因素,需要控制变量,故Ⅱ中也是5mL15%的过氧化氢溶液,烧杯中右侧导管口产生气泡的速率比左侧快,说明反应速率与反应物的浓度有关,过氧化氢在二氧化锰的催化作用下反应生成水和氧气,故填:5;反应物浓度;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$ 2H2O+O2↑;
甲中镁与盐酸反应生成氯化镁,故甲中流入烧杯中的溶质有氯化镁和氯化氢,氢氧化钠溶于水放出大量的热,导致温度升高,压强大于大气压,故乙中的液体会流入烧杯中,故填:氢氧化钠溶于水,放出热量,使得瓶内压强大于外界压强;MgCl2 HCl.
点评 本题考查的是化学实验的设计,完成此题,可以依据已有的知识进行.


科目:初中化学 来源: 题型:选择题
| A. | 硫酸铜溶液中铜离子和硫酸根离子的电荷总数相等 | |
| B. | CuSO4•5H2O是一种特殊的混合物 | |
| C. | 胆矾遇水能变蓝色,故可用胆矾来检验水的存在 | |
| D. | 金属钠放入硫酸铜溶液中有红色的铜被置换出 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
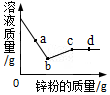 向一定量硝酸银和硝酸铜的混合溶液中加入锌粉,所得溶液的质量与加入锌粉的质量关系如图所示.下列说法正确的是( )
向一定量硝酸银和硝酸铜的混合溶液中加入锌粉,所得溶液的质量与加入锌粉的质量关系如图所示.下列说法正确的是( )| A. | a点所得溶液中的溶质是硝酸铜、硝酸锌 | |
| B. | 向b点所得固体中加入盐酸有气泡产生 | |
| C. | c点所得固体为银和铜 | |
| D. | d点所得溶液中溶质一定有硝酸锌,可能有硝酸铜 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 农业生产与化学知识紧密相关.
农业生产与化学知识紧密相关.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 向某固体中加入稀盐酸有气泡产生,可证明该物质中一定含有CO32- | |
| B. | 可用过量的Cu(OH)2除去CuSO4溶液中少量的H2SO4 | |
| C. | 常温下可用Fe与AgCl反应制取Ag | |
| D. | 将Fe、Cu、Ag放入稀盐酸中,可确定它们的活动性顺序 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com