合理利用化学反应可以造福人类.请写出下列相关的化学反应方程式并完成题后填空:
(1)高锰酸钾制氧气______.
(2)“湿法炼铜”的原理是______;反应后溶液的质量要比反应前溶液的质量______.(填“大”、“小”或“相等”)
(3)用稀盐酸除去铁制品表面的铁锈时,发生的反应为______;铁锈溶解后的溶液呈______色;反应一会儿后,还会看到铁制品表面有______(填现象),反应的方程式______,该反应基本类型是______反应.
(4)反应条件是控制实验的灵魂,相同的反应物在不同的反应条件下可能会生成不同的产物.二氧化碳和水在不同条件下发生反应,产物不同.写出相应的方程式:______、______.
解:(1)高锰酸钾在加热条件下反应生成锰酸钾、二氧化锰和氧气.该反应的化学方程式为:2KMnO
4
K
2MnO
4+MnO
2+O
2↑.
(2)湿法冶金炼铜就是铁和硫酸铜溶液反应,生成硫酸亚铁和铜,故答案为:Fe+CuS0
4=Cu+FeSO
4.因为铜的相对原子质量大于铁的相对原子质量,故反应后溶液的质量减小.
(3)铁锈的主要成分是氧化铁,铁锈和盐酸反应能生成氯化铁和水,故答案为:6HCl+Fe
2O
3═2FeCl
3+3H
2O;铁离子的颜色为黄色,故铁锈溶解后的溶液呈黄色;
铁锈溶解后,铁与盐酸继续反应生成氯化亚铁和氢气,故反应一会儿后,还会看到铁制品表面有气泡生成,反应的方程式为:Fe+2HCl═FeCl
2+H
2↑;该反应为一种单质和一种化合物反应生成另一种单质和另一种化合物,故属于置换反应;
(4)二氧化碳与水反应生成碳酸,能使紫色石蕊试液变红,反应的化学方程式为:CO
2+H
2O=H
2CO
3;植物光合作用能将二氧化碳和水转化成葡萄糖和氧气,反应的化学方程式为:6CO
2+6H
2O
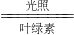
C
6H
12O
6+6O
2.
故答案为:(1)2KMnO
4
K
2MnO
4+MnO
2+O
2↑;(2)Fe+CuS0
4=Cu+FeSO
4;小;(3)6HCl+Fe
2O
3═2FeCl
3+3H
2O;黄;气泡;Fe+2HCl═FeCl
2+H
2↑;置换;
(4)CO
2+H
2O=H
2CO
3;6CO
2+6H
2O
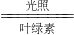
C
6H
12O
6+6O
2分析:书写化学方程式时,必须熟悉反应物、生成物和反应条件,必须遵守质量守恒定律,依据客观事实.
根据四种基本反应类型的概念和特征分析反应类型.
点评:解答本题要求学生掌握教材中所学习的化学知识并能熟练书写化学方程式,只有这样才能对相关方面的问题做出正确的判断.

 K2MnO4+MnO2+O2↑.
K2MnO4+MnO2+O2↑.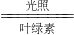 C6H12O6+6O2.
C6H12O6+6O2. K2MnO4+MnO2+O2↑;(2)Fe+CuS04=Cu+FeSO4;小;(3)6HCl+Fe2O3═2FeCl3+3H2O;黄;气泡;Fe+2HCl═FeCl2+H2↑;置换;
K2MnO4+MnO2+O2↑;(2)Fe+CuS04=Cu+FeSO4;小;(3)6HCl+Fe2O3═2FeCl3+3H2O;黄;气泡;Fe+2HCl═FeCl2+H2↑;置换;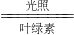 C6H12O6+6O2
C6H12O6+6O2

 特高级教师点拨系列答案
特高级教师点拨系列答案