
【题目】同学们利用“硫酸、硝酸铵、氢氧化钠、碳酸钾”四种物质的溶液进行探究学习,完成下列各问:
【实验探究】
(1)A、B、C、D四组同学分别进行了下列实验
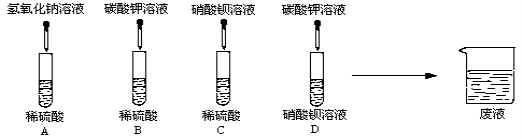
写出下列的两个化学方程式:
①A中的反应 。
②D中的反应 。
【挖掘实质】
下图是A组反应的微观过程示意图该化学反应的实质可以表示为H++OH-=H2O
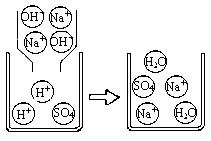
【实践运用】
完成试验后,四组同学将废液倒入同一个烧杯中,再将废液过滤,得到无色溶液和白色沉淀,用无色溶液滴加紫色石蕊试剂,变为红色。
(1)①溶液中的白色沉淀一定是 ,理由是 。
(2)废液中一定不含有的离子是 。
(3)为了验证该溶液中可能含有的离子是否存在,我设计如下实验进行验证
溶液中可能含有的离子 | 实验步骤 | 实验现象 | 实验结论 |
可能含有 | ②取滤液滴加 | 现象明显 | 含有该离子 |
【答案】(1)①H2SO4+2NaOH==Na2SO4+2H2O
②K2CO3+Ba(NO3)2==BaCO3↓+2KNO3
【实践运用】(1)硫酸钡。BaSO4与酸不反应,而BaCO3要与酸反应
(2)OH- CO32-
(3)可能含硫酸根离子
溶液中可能有的离子 | 实验步骤 |
①可能含硫酸根离子 | ②向滤液中加入硝酸钡(或氯化钡、氢氧化钡等) |
(二)可能含钡离子
溶液中可能有的离子 | 实验步骤 |
①可能含钡离子 | ②向溶液中加入稀硫酸(或硫酸钠等)溶液 |
【解析】
试题分析:(1)①根据图示可知:试管A中的稀硫酸能与加入的氢氧化钠中和反应生成盐和水,化学方程式为:H2SO4+2NaOH==Na2SO4+2H2O
②D为碳酸钾加入硝酸钡中,二者可发生复分解反应生成碳酸钡沉淀和硝酸钾,反应的化学方程式为:K2CO3+Ba(NO3)2==BaCO3↓+2KNO3
【实践运用】
(1)因题目中的反应发生在硫酸、氢氧化钠、硝酸钡和碳酸钾之间;其中氢氧根离子能和氢离子结合形成水分子(A中);碳酸根离子可与氢离子结合形成水分子和二氧化碳分子(B中);碳酸根离子也可与钡离子结合形成碳酸钡沉淀(D中)。当“废液中出现白色沉淀”时,该沉淀一定为钡的沉淀。其中硫酸钡和碳酸钡均为沉淀。由于 “加入紫色石蕊试液时,变为红色”,说明溶液呈酸性,即含较多的氢离子。因为碳酸钡可与酸反应,而硫酸钡不与酸反应。所以沉淀只有硫酸钡。
(2)向溶液中“加入紫色石蕊试液时,变为红色”,说明溶液呈酸性,即含较多的氢离子。由于氢离子能和氢氧根离子结合形成水分子;可与碳酸根离子结合形成水分子和二氧化碳分子;所以氢氧根离子和碳酸根离子一定不存在。
(3)根据题意可知:钠离子和硝酸根离子未形成沉淀或气体,所以一定存在于所得的溶液中。结合上面的分析可知:所得溶液中一定含氢离子、钠离子和硝酸根离子,一定不含氢氧根离子和碳酸根离子。而在“实践运用”中所得的沉淀是由硫酸根离子和钡离子形成的。所以无法确定所得到的溶液中是否含硫酸根离子或钡离子。即溶液中可能含的离子为硫酸根离子或钡离子(二者只含其一)。因此,实验应为:
(一)可能含硫酸根离子
溶液中可能有的离子 | 实验步骤 |
①可能含硫酸根离子 | ②向滤液中加入硝酸钡(或氯化钡、氢氧化钡等) |
(二)可能含钡离子
溶液中可能有的离子 | 实验步骤 |
①可能含钡离子 | ②向溶液中加入稀硫酸(或硫酸钠等)溶液 |


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:初中化学 来源: 题型:
【题目】(6分)下图所示是Ca(OH)2的部分性质实验,回答有关问题。
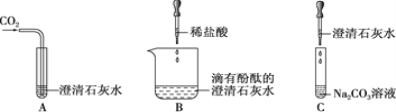
(1)A中的实验现象是 。
(2)C中的实验现象是 ;发生反应的化学方程式为 。
(3)将这三个实验后的所有物质倒入同一洁净的烧杯中,静置,观察到上层溶液为无色,底部有白色沉淀。取少量上层溶液与足量稀盐酸混合,无明显现象。综合分析可知:上层溶液中一定含有的溶质是酚酞和 ,可能含有的溶质是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是甲、乙、丙三种物质的溶解度曲线。下列说法错误的是
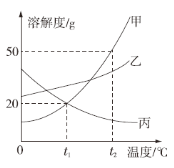
A、要配制相同质量分数的甲、丙两种物质的饱和溶液,应该将温度控制在t1 ℃
B、t2 ℃时,将30 g甲物质加入到50 g水中不断搅拌,形成的溶液的质量是80g
C、要从甲物质的饱和溶液中获得晶体甲,可采用降温结晶的方法
D、将丙物质的饱和溶液转化为不饱和溶液可以采用加水或降温的方法
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学反应前后,下列各项中,肯定没有变化的是
①原子数目 ②分子数目 ③元素的种类 ④物质的总质量 ⑤物质的种类 ⑥原子的种类
A.①②③④⑤⑥ B.①③④⑥ C.①④⑥ D.①③⑤
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列各组溶液,不加任何试剂就能鉴别出的是
A.Na2SO4 、BaCl2 、KNO3 、NaCl
B.Na2SO4 、K2CO3、 BaCl2、 HCl
C.NaOH、 MgSO4、 FeCl3 、BaCl2
D.CuCl2、 AgNO3、 NaNO3 、HCl
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】【改编】(8分)请你完成对实验室制取二氧化碳的实验探究。
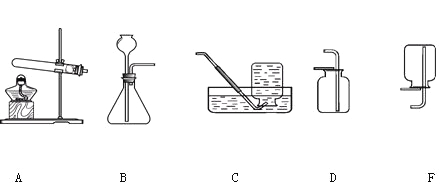
(1)选择药品。下表是对四组药品进行实验的记录:
组别 | 药品 | 实验现象 |
① | 块状石灰石和稀盐酸 | 产生气泡速率适中 |
② | 石灰石粉末和稀盐酸 | 产生气泡速率很快 |
③ | 块状石灰石和稀硫酸 | 产生气泡速率缓慢并逐渐停止 |
④ | 碳酸钠粉末和稀盐酸 | 产生气泡速率很快 |
从制取和收集的角度分析,一般选择第 组药品(填字母序号,下同),该组药品发生反应的化学方程式为 (2分)。可选用制取装置为 ;
(2)选择D装置收集二氧化碳,其验满方法是 。
(3)气体检验。将生成的气体通入紫色石蕊溶液中,溶液变红,确定该气体是二氧化碳。这种检验方法是否正确?若正确请说明理由,若不正确请写出正确的检验方法 。
(4)若选用AC作为制取氧气装置,那么可用 (化学方程式,2分)制取
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(10分)某学校化学兴趣小组的同学想测定赤铁矿中氧化铁的含量,做了如下实验:首先称取100 g该赤铁矿样品放入烧杯中,然后将500g的稀盐酸分5次加入烧杯内(假设其余杂质均不与盐酸反应也不溶于水)进行充分反应.实验过程中的数据记录如下:
第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
稀盐酸的质量 | 100g | 100g | 100g | 100g | 100g |
溶液的质量 | 116.0g | X | 348.0g | 464.0g | 575.0g |
请回答下列问题:
(1)该小组要用质量分数为36.5%浓盐酸配制所需的500g的稀盐酸,则需浓盐酸的质量为_____
(2)写出实验中发生反应的化学方程式____________________
(3)列出求解生成氯化铁总质量的比例式____________________
(4)将第二次反应后所得溶液蒸发掉32g水(未达到饱和),则所得溶液的溶质质量分数是________
(5)某工厂要想制得420t含杂质3%的生铁,需要这种赤铁矿的质量为___________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com